Prema funkcije kisika su skupina od organski spojevi koji imaju atome kisika vezane za ugljikov lanac. Jesu li oni:
alkohol;
keton;
aldehid;
karboksilna kiselina;
ester;
eter.
Pročitajte također:Ugljikovodici — spojevi sastavljeni od ugljika i vodika
Sažetak o funkciji kisika
Kisikove funkcije su skupina spojeva koji sadrže atom kisika. kisik vezani izravno na ugljikov lanac.
Različite funkcije kisika karakterizirane su specifičnim strukturnim rasporedom atomi, koja se naziva funkcionalna grupa.
Funkcionalne skupine odgovorne su za svojstva svake organske funkcije.
Kisikove funkcije su: alkohol, keton, aldehid, karboksilna kiselina, ester i eter.
Video lekcija o funkciji kisika
Koje su funkcije kisika?
Tijelesne funkcije obogaćene kisikom su one koje imaju atom kisika vezan na atom kisika ugljik ugljikovog lanca.
Funkcije kisika su:
alkohol;
keton;
aldehid;
karboksilna kiselina;
ester;
eter.
Organske funkcije identificiraju se svojom funkcionalnom skupinom, što je strukturni raspored atoma ili veza, odgovoran za karakteristična svojstva tog skupa spojeva.
Važnost kisikovih funkcija
Prisutnost kisikovih funkcija u organskim spojevima može promijeniti svojstva spojeva, u usporedbi s odgovarajućim ugljikovodikom, s jednakim brojem ugljika.
Funkcije kisika karakterizirane su pojavom hidroksilnih, karbonilnih ili karboksilnih skupina. A prisutnost atoma kisika povećava polarni karakter spojeva, čineći ih hidrofilnijima, odnosno povećavajući njihov afinitet prema voda.
Pojava funkcija kisika također je odgovoran za vrstu međumolekularna siladjelujući između molekula. Priroda i intenzitet međumolekulskih sila utječu na topljivost te temperature taljenja i vrenja.
Donja tablica donosi usporedbu nekih svojstava triju spojeva koji imaju isti broj atoma ugljika, ali se razlikuju po prisutnosti oksigeniranih funkcionalnih skupina.
Organski kompost | |||
Butan (C4H10) |
Butanon (C4H8O) |
Butanol (C4H10O) |
|
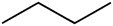 |
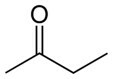 |
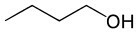 |
|
organska funkcija |
Ugljikovodik |
keton (funkcija kisika) |
Alkohol (funkcija kisika) |
Polaritet |
apolaran |
Polarni |
Polarni |
temperatura topljenja |
-138,3°C |
-86°C |
-89°C |
temperatura vrenja |
-0,5°C |
80°C |
118°C |
Prevladavajuća međumolekulska sila |
Inducirani dipol |
stalni dipol |
vodikove veze |
Alkohol
Organska funkcija alkohola ima hidroksilnu skupinu (-OH) vezanu izravno na zasićeni ugljik, odnosno onaj ugljikov atom koji uspostavlja samo jednostruke veze.
Funkcionalna skupina alkohola: R-OH (hidroksil).
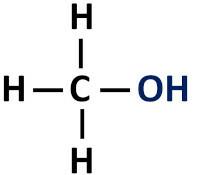
alkoholi su klasificirani prema vrsti ugljika na koji je hidroksil vezan. Primarni alkoholi imaju hidroksil vezan za primarni ugljik. Sekundarni alkoholi imaju hidroksilnu skupinu vezanu na sekundarni ugljik, a tercijarni alkoholi imaju svoju -OH skupinu vezanu na tercijarni ugljik.
Organski spoj koji ima samo jedan hidroksil naziva se monoalkohol. Ako ima dvije hidroksilne skupine, naziva se dialkohol. Iznad toga, molekule se nazivaju polialkoholi.
A nomenklatura za alkohole slijedi preporuku Iupac-a (International Union of Pure and Applied Chemistry), razmatrajući sklapanje imena kemijskih struktura u tri dijela:
Prefiks – povezan s brojem ugljika.
Infiks – odnosi se na vrstu kemijske veze uspostavljene između atoma ugljika.
Sufiks – vezan uz funkcionalnu skupinu. U slučaju alkohola, sufiks koji se koristi je -zdravo.
Pogledajte primjere:
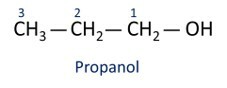
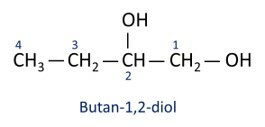
O glavni alkohol je etanl (CH3CH2OH), koristi se kao gorivo, u alkoholnim pićima, kao kemijsko otapalo, sredstvo za čišćenje i dezinfekciju.
keton
Funkcija organskog ketona odgovara karbonilna funkcionalna skupina (C=O), smještena između dva ugljikova atoma ugljikovog lanca.
Funkcionalna skupina ketona: R1–(C=O)–R2.

Ketoni su klasificirani prema broju karbonilnih skupina:
Monoketoni – imaju jednu karbonilnu skupinu.
Diketoni – imaju dvije karbonilne skupine.
Politoni – imaju više od dvije karbonilne skupine.
A nomenklatura za ketone slijedi pravila Iupac, ali s razlikom u pisanju sufiksa. Ketoni se identificiraju sufiksom -ona.
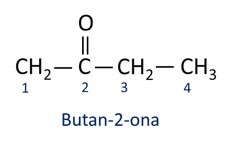
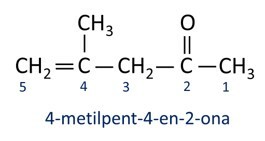
Općenito, ketoni nalaze primjenu u proizvodnji drugih kemikalija i lijekova. U industriji se ketoni koriste kao otapala za boje, boje i lakove. Jedan od najpoznatijih ketona je propanon, koji je u narodu poznat kao aceton. Za skidanje laka za nokte koriste se otopine acetona.
Pročitajte također:Amidi — spojevi koji imaju dušik vezan na karbonil
Aldehid
Funkcija organskog aldehida je karakteriziran prisutnošću karbonilne funkcionalne skupine, čiji ugljikov atom ima vodikovu vezu.
Funkcionalna skupina aldehida: H–C=O (formil).
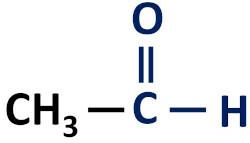
Aldehidi se uvijek pojavljuju na kraju ugljikovih lanaca jer njihov atom ugljika mora biti vezan na barem jedan atom vodika.
A nomenklatura za aldehidne spojeve slijedi IUPAC pravila, razlikuju se po sufiksu. Aldehidi se identificiraju sufiksom -al.
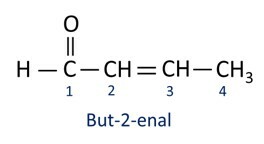
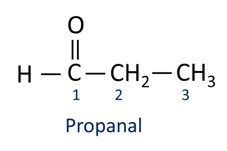
Aldehidi se industrijski koriste u proizvodnji parfema i aroma, jer njegov miris i okus variraju ovisno o duljini ugljikovog lanca. Aldehidni spojevi također se koriste u proizvodnji proizvoda za čišćenje, lijekova, polimera, između ostalog. Aldehidi kratkog ugljičnog lanca mogu se koristiti kao sredstvo za konzerviranje, poput poznatog formalin, koji je aldehid nazvan metanal.

karboksilna kiselina
Funkcija organske karboksilne kiseline identificira se prisutnošću karboksilne funkcionalne skupine (-COOH).
Funkcionalna skupina karboksilnih kiselina: –(C=O)OH ili –COOH.

Spojevi koji pripadaju ovoj organskoj funkciji su slabe kiseline jer lako otpuštaju H ione+ u vodenoj otopini.
A nomenklatura za karboksilne kiseline slijedi Iupac pravila, međutim izraz "kiselina" pojavljuje se ispred prefiksa koji označava broj ugljika, a korišteni sufiks je -oic.
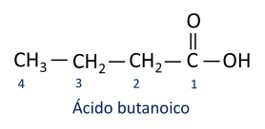
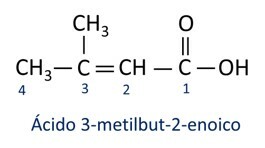
O najčešća karboksilna kiselina u svakodnevnom životu je Octena kiselina, tvar prisutna u octu. Vitamin C, kojim obiluju mnogi citrusi, organska je molekula koja se naziva askorbinska kiselina.
Ester
Funkcija organskog estera identificira se prisutnošću karbonilne funkcionalne skupine, čiji atom ugljika ima ligand kisika.
Funkcionalna skupina estera: –R–(C=O)O–R'.
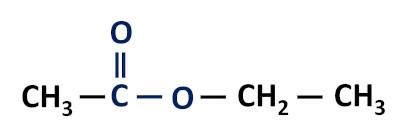
Esteri su derivati karboksilnih kiselina, razlikuju se od ovih po tome što imaju alkilni radikal vezan za atom kisika umjesto za atom vodika.
Molekule koje pripadaju esterskoj funkciji nastaju reakcijom između karboksilne kiseline i alkohola, reakcija poznata kao esterifikacija.
Pravila za nomenklatura estera definirao Iupac smatraju da se molekula sastoji od dva dijela:
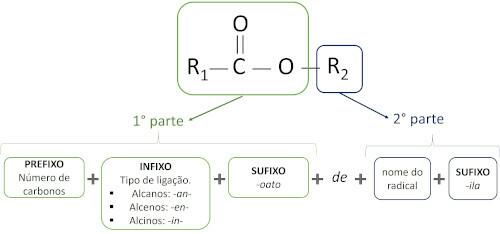
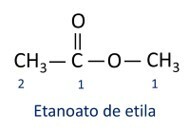
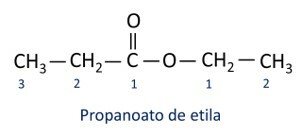
Glavna karakteristika estera je njihova sposobnost simulacije okusa i mirisa prirodne hrane, prema duljini ugljikovih lanaca (R1 i R2). Zbog toga se esteri naširoko koriste kao arome u prehrambenoj industriji, u proizvodnji lijekova, parfema i kozmetike.
Eter
Organska funkcija etera je karakteriziran time što ima atom kisika između dva ugljikova lanca.
Funkcionalna skupina etera: R–O–R.

Eteri su vrlo zapaljive tvari, karakterističnog i jakog mirisa.
A službena Iupac nomenklatura za etere slijedi redoslijed prefiks + infiks + sufiks. Međutim, strani molekule koja ima manje ugljika daje se sufiks -oksi dok se duži ugljikov lanac naziva kao da je ugljikovodik, dobivajući sufiks -o.
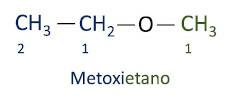
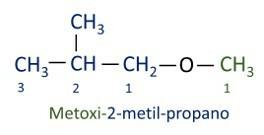
Eteri su koriste se kao otapala za boje, smole, ulja i masti. Zbog toga se koriste u različitim industrijskim i farmaceutskim procesima. Eter se nekoć koristio kao anestetik, a danas su ga zamijenile druge sigurnije tvari.
Pročitajte također:Nitro spojevi — spojevi koji sadrže nitro (NO2) skupine u svojoj molekuli
Riješene vježbe o funkcijama kisika
Pitanje 1
(Uece) U organskoj kemiji funkcionalna skupina definirana je kao molekularna struktura koja daje tvarima slično kemijsko ponašanje. Skup spojeva koji imaju istu funkcionalnu skupinu naziva se organska funkcija. Označite opciju koja točno prikazuje spoj i organsku funkciju kojoj pripada.

rezolucija:
Slovo C
Među alternativama, jedina koja ispravno izražava funkcionalnu skupinu u nazivu kemijske funkcije je točka C. Organska esterska funkcija definirana je karbonilnom funkcionalnom skupinom, čiji ugljikov atom također ima kisikov ligand.
U točki A izražena je eterska funkcionalna skupina.
U točki B izražena je ketonska funkcionalna skupina.
U točki D izražena je amidna funkcionalna skupina. amini to je amidi pripadaju dušikovim funkcijama.
pitanje 2
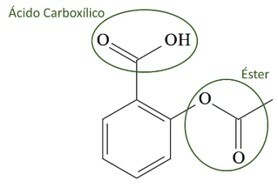
(UCS-RS) U 5. st. pr. C., Hipokrat, grčki liječnik, napisao je da proizvod od kore vrbe ublažava bol i snižava temperaturu. Taj isti proizvod, kiseli prah, čak se spominje u tekstovima iz drevnih civilizacija Bliskog istoka, Sumera, Egipta i Asirije. Američki domoroci koristili su ga i protiv glavobolje, groznice, reume i drhtavice. Ovaj lijek je prethodnik aspirina, čija je kemijska struktura prikazana u nastavku.
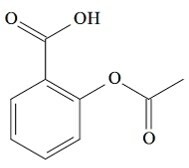
Organske funkcije prisutne u strukturi aspirina, predstavljene gore, su:
a) karboksilna kiselina i ester.
b) alkohol i eter.
c) amin i amid.
d) amin i eter.
e) aminokiselina i alkohol.
rezolucija:
Slovo A
Ana Luiza Lorenzen Lima
Profesor kemije
Izvor: Brazilska škola - https://brasilescola.uol.com.br/quimica/funcoes-oxigenadas.htm
