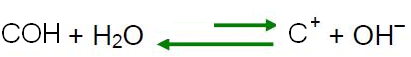
Medij se smatra neutralnim ako ima istu koncentraciju, u mol/L, hidronijevih iona (H3O+) i hidroksid (OH-).
Primjer neutralnog medija koji čak služi i kao standard za druge otopine je čista destilirana voda na temperaturi od 25ºC. Na ovoj temperaturi ima točno 1. 10-7 mol/L oba iona. Dakle, vaš ionski proizvod (Kw) jednako je 10-14 (mol/L)2:
Kw = [H3O+]. [Oh-]
Kw = (1. 10-7 mol/L). (1. 10-7 mol/L) = 10-14 (mol/L)2
pH i pOH su dati u nastavku:
pH= - log [H3O+] pOH= -log[OH-]
pH= - log 1. 10-7 pOH= - log 1. 10-7
pH = 7pOH = 7
To nam pokazuje da je u neutralnom rješenju pH je jednak pOH.
- kiseli medij:
U kiselom mediju koncentracija H iona3O+ veći je od OH iona-.
Takvo rješenje može se postići dodavanjem malog dijela H iona3O+na primjer, pomoću kiseline.
Prema Le Chatelierovom principu, kada se sustavu u ravnoteži izazove poremećaj, on se teži ponovnom prilagođavanju kako bi smanjio učinke ove sile. To znači da ako se vodi doda kiselina, H ioni3O+ oni će biti u višku i ravnoteža će se pomaknuti u smjeru obrnutog reakcije, ulijevo. Dakle, ovi suvišni ioni će reagirati s OH ionima
-. Dakle, koncentracija OH iona- će se smanjiti i otopina će postati kisela.
Ionski produkt (Kw) uvijek je jednak 10-14, ali koncentracija H iona3O+ veća je od koncentracije OH iona-1. Dakle, pH je veći od pOH u kiselom mediju, ali njegov zbroj uvijek je jednak 14.
Također, veća je koncentracija H iona3O+, veća je pH vrijednost. Na sobnoj temperaturi (25°C), pH < 7 i pOH > 7.

- Osnovno znači:
U bazičnom mediju koncentracija OH iona- je veći od H iona3O+.
Ako vodi dodamo bazu, to znači da dodajemo OH ione.- i, kako je objašnjeno u prethodnoj točki, Le Chatelierovim principom, ravnoteža reakcije samoionizacija vode kretat će se u suprotnom smjeru, a višak iona će reagirati s H ioni3O+, smanjujući vašu koncentraciju i čineći otopinu bazičnom.
U tom slučaju, pOH će biti veći od pH. Na sobnoj temperaturi (25°C), pH > 7 i pOH < 7.

Kratko:
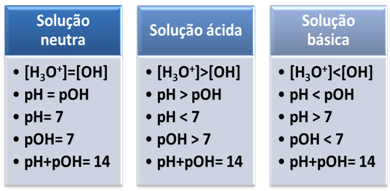
Autora Jennifer Fogaça
Diplomirao kemiju

