Hessov zakon stvorio je švicarski kemičar Germain H. Hess (1802-1850), koji se smatra jednim od utemeljitelja termokemije. Njegov je zakon rekao:

Odnosno, ΔH ovisi samo o vrijednosti entalpije reagensa i proizvoda, kao u izrazu:
| ΔH = ΔHreagensi + ΔHproizvoda |
Na primjer, razmotrite reakciju gdje 1 mol vode (H2O) pretvara se u vodu u plinovitom stanju. Ova se reakcija izvodi dva puta; međutim, izabrani su različiti putovi:
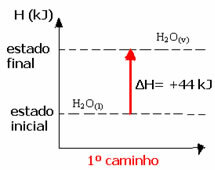
(1.) Izvedeno je u jednom koraku:
H2O(1) → H2O(v) ΔH = +44 kJ
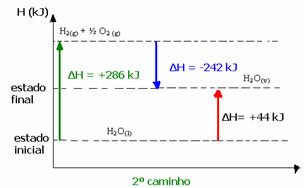
(2.) Provedeno je u dvije faze:
1. korak: H2O(1) → H2 (g) + ½2 (g) ΔH = +286 kJ
2. faza: H2 (g) + ½2 (g) → H2O(v) ΔH = -242 kJ
H2O(1) → H2O(v) ΔH = +44 kJ
Imajte na umu da bez obzira je li izveden jedan ili dva koraka, promjena entalpije (ΔH) uvijek iznosi 44 kJ. To je zato što je ΔH algebarski zbroj vrijednosti valoresH koraka koji čine proces, odnosno međuprocesa:
| ΔH = ΔH1 + ΔH2 + ΔH3 + ... |
Primjerice, u drugom je slučaju ukupni ΔH reakcije bio zbroj ΔH prvog koraka (ΔH = +286 kJ) s onim drugog (ΔH = -242 kJ). Dakle, dobili smo istu vrijednost reakcije u jednom koraku:
ΔH = (+286 + (-242)) kJ
ΔH = (+286 -242) kJ
ΔH = +44 kJ
Stoga nas zanimaju samo početne i konačne vrijednosti. U ovom slučaju početno stanje odgovara H2O(1) i kraj do H2O(v).
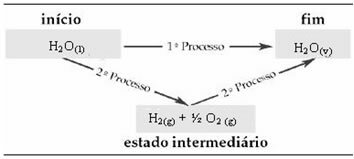
Ovaj je zakon postao vrlo važan u termokemiji, jer se određenim kemijskim reakcijama ne može eksperimentalno odrediti ΔH. Međutim, prema Hessovom zakonu entalpija ove vrste reakcije može se izračunati iz entalpija drugih reakcija (intermedijarne reakcije).
Napisala Jennifer Fogaça
Diplomirao kemiju
Brazilski školski tim