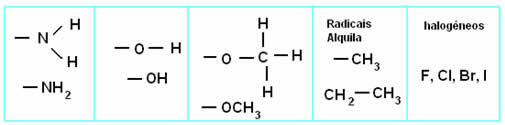
Acetilen ili etin ugljikovodik je prepoznat kao najjednostavniji i najvažniji alkin u skupini.
Sastoji se od samo dva atoma vodika i dva atoma ugljika: C2H2.
Njihovi atomi spojeni su trostrukom vezom, koja karakterizira alkine.
Strukturna formula acetilena je .
Značajke
Na sobnoj temperaturi, acetilen je plin bez boje i mirisa u svom čistom obliku.
Kad se pomiješa s drugim tvarima, ima karakterističan i neugodan miris zbog prisutnih nečistoća.
Plin acetilen ima malu topljivost u vodi, jer je topiv u organskim spojevima.
Kada se zagrije ili pomiješa sa zrakom, acetilen postaje izuzetno zapaljiv.
Acetilen za biće alkin je reaktivniji od alkani i alkeni.
Kako se proizvodi?
Najjednostavniji i najčešće korišten postupak za proizvodnju acetilena je sljedeća kemijska reakcija između kalcijevog karbida (CaC2) i vode (H2O):
Tijekom procesa nastaje kalcijev hidroksid (Ca (OH)2) i plin acetilen (C2H2).
Ova reakcija je egzotermna, odnosno oslobađa puno topline koja se mora ukloniti kako bi spriječila eksploziju acetilena.
Acetilen se još uvijek može dobiti pucanjem Nafta, gdje se prisutni ugljikovodici raščlanjuju na manje dijelove.
Saznajte više o Ugljikovodici.
Čemu služi?
Acetilen ima nekoliko namjena u industriji, od njega nastaju brojni spojevi.
Njegova glavna upotreba je kao sirovina za proizvodnju plastike, tekstilnih vlakana i sintetičke gume.
neke vrste polimeri poput PVC-a (polivinilklorid) i PVA (polivinil acetat) također se dobivaju preko acetilena.
Također se koristi za rezanje metala pomoću puhalice i u proizvodnji predmeta od stakla.
Neko se vrijeme koristio za osvjetljavanje mjesta bez električne energije, jer kada se sagorijeva s odgovarajućom količinom zraka stvara bijelu svjetlost.
Pročitajte i vi:
- Organska kemija
- Kemijske reakcije