Hibridizacija je naziv za fuziju ili uniju nepotpunih atomskih orbitala, pojavu koja povećava broj kovalentne veze što atom može učiniti. Sjetimo se da je orbitala područje atoma u kojem postoji veća vjerojatnost pronalaska elektrona.
Znati broj veza koje atom stvara i razumjeti fenomen hibridizacija, potrebno je znati neke temeljne točke o atomu:
1O točka: podrazini energije
Podrazini energije koje atom može imati su s, p, d, f.
2O točka: broj orbitala po podrazini
Svaki podnivo energije ima različitu količinu orbitala, kao što možemo vidjeti dolje:
Podrazina s: 1 orbitala;
p podnivo: 3 orbitale;
Podrazina d: 5 orbitala.
Generički prikaz ovih orbitala vrši se na sljedeći način:
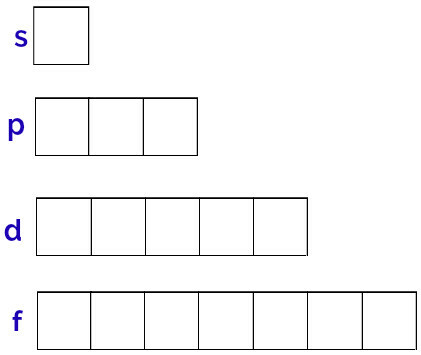
Prikaz orbitala svakog podrazine
Prema Pauliju, orbitala može imati najviše 2 elektrona, sa vrti se (rotacijski pokreti) suprotno.
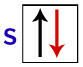
Prikaz s orbite s njezinim elektronima
Prema Hundu, orbitala podrazine prima svoj drugi elektron tek kad su sve ostale orbitale tog podrazine već primile prvi elektron.
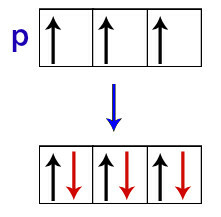
Raspodjela elektrona u p podrazinama orbitala
3O točka: elektronička distribucija
Da bismo razumjeli hibridizaciju i broj veza koje atom stvara, bitno je provesti elektronska distribucija na Linusovom Paulingovom dijagramu.

Dijagram Linusa Paulinga
Imajući na umu da je maksimalni broj elektrona u svakom podrazini:
s = 2 elektrona;
p = 6 elektrona;
d = 10 elektrona;
-
f = 14 elektrona.
Ne zaustavljaj se sada... Ima još toga nakon oglašavanja;)
Nakon ovog kratkog pregleda, sada možemo definirati što je hibridizacija. Za to ćemo upotrijebiti kemijski element bor (atomski broj = 5) kao primjer.
Kada vršimo elektroničku distribuciju bora, imamo:
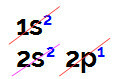
Elektronička raspodjela bora u Linusovom Paulingovom dijagramu
U ovoj raspodjeli moguće je primijetiti da bor ima 2 elektrona u s podrazini i 1 elektron u podrazinu p valentni sloj.
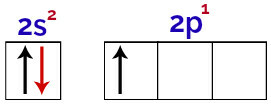
Elektroni u orbitalama valentnog sloja bora
Kako bor ima 1 nepotpunu orbitalu, stoga bi trebao stvoriti samo jednu kovalentnu vezu, jer je broj veza uvijek izravno povezan s brojem nepotpunih orbitala.
Dakle, kada atom bora prima energiju iz vanjske okoline, njegovi se elektroni, posebno oni u valentnoj ljusci, pobuđuju. To uzrokuje da jedan od elektrona iz s orbitale napusti i zauzme jednu od praznih p orbitala, što rezultira 3 nepotpune atomske orbitale, kao što možete vidjeti na sljedećoj slici:

Prikaz pobuđenog stanja atoma bora
Napokon, postoji sjedinjenje nepotpune orbitale s nepotpunim p orbitalama. Taj se sindikat zove hibridizacija. Budući da imamo fuziju s orbitale s dva p, ona se naziva hibridizacija sp2.
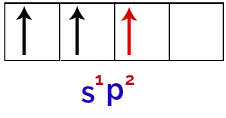
Prikaz hibridiziranih orbitala u atomu bora
Pored bora, nekoliko drugih kemijskih elemenata prolazi kroz fenomen hibridizacije, poput sumpora (S), ksenona (Xe), fosfor (P), ugljik (Ç), berilijum (Biti).
Ja, Diogo Lopes Dias
Želite li uputiti ovaj tekst u školskom ili akademskom radu? Izgled:
DANI, Diogo Lopes. "Što je hibridizacija?"; Brazil škola. Dostupno u: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-hibridizacao.htm. Pristupljeno 27. lipnja 2021.
Energija vezanja, Kemijske reakcije, prekidanje veza, proučavanje varijacija energije, entalpijska varijacija reakcija, opskrba energijom, prekid veze reagensa, endotermni proces, oslobađanje energije, energija oslobođena u formacija
