Na reakcije izgaranja prisutni su u mnogim aspektima našeg svakodnevnog života. Na primjer, glavni izvori energije proizlaze izgaranjem ili izgaranjem određenih goriva, poput etanola, benzina, ugljena, između ostalog. Nadalje, energija koja nam je potrebna za preživljavanje i obavljanje posla rezultat je reakcija izgaranja koje se odvijaju u našim stanicama kada "sagorijevamo" hranu koju jedemo.
Ali što je potrebno da se dobije reakcija izgaranja?
Potrebne su tri stvari:
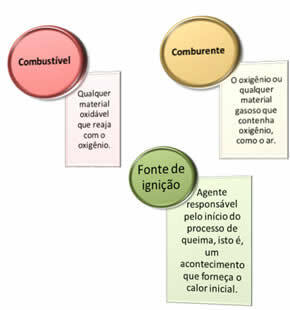
Ova tri čimbenika čine vatreni trokut, jer nakon što započne reakcija izgaranja, oslobođena energija održava reakciju i omogućuje joj nastavak sve dok gorivo, oksidans ili toplina (oslobođena energija) ne nestanu. To znači da će postojati Lančana reakcija.
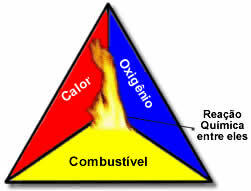
Na primjer, ako netko baci zapaljenu cigaretu u šumu, doći će do požara (reakcija izgaranja). U ovom slučaju, Grm to je gorivo, O kisik prisutan u zraku atmosferski je oksidans to je cigareta upaljeno je bilo izvor paljenja. Spaljivanje će se nastaviti dok se ne ukloni jedan od tri čimbenika. Ako vatrogasci bace vodu, vrućina će biti uklonjena. Ali čak i ako se ništa ne poduzme kako bi se zaustavilo ovo izgaranje, ono će završiti u nekom trenutku, odnosno kad gorivo (šuma) ponestane.
Kao što je već spomenuto, u tim se reakcijama oslobađa toplina, pa je izgaranje egzotermna reakcija. Međutim, ova vrsta reakcije je nepotpuno izgaranje. Da biste razumjeli zašto, pogledajte razliku između potpunog i nepotpunog izgaranja:
Ne zaustavljaj se sada... Ima još toga nakon oglašavanja;)
Potpuno izgaranje:
Analizirajući organske spojeve kao goriva, moramo:
| THE potpuno izgaranje dogodit će se kad se ugljikov lanac prekine i svi atomi ugljika u ugljikovom lancu potpuno oksidiraju. |
| Vas oblikovani proizvodi ugljikovodicima bit će CO2 (ugljični dioksid) i H2O (Voda). |
Promatrajte potpuno izgaranje izoktana, koji je jedna od komponenata benzina.
Ç8H18 (g) +25/2 O.2 (g) → 8 CO2 (g) + 9 sati ujutro2O(1)
Nepotpuno izgaranje
| U ovom slučaju nema dovoljno oksidansa, odnosno dovoljno kisika da sagori svo gorivo. |
| Dakle, nastali proizvodi su CO (ugljični monoksid) i H2O. |
Primijetite isto sagorijevanje izoktana, međutim, sada nepotpuno:
Ç8H18 (g) + 17/2 O.2(g) → 8 CO (g) + 9 sati ujutro2O(1)
Primjer je paljenja šuma, jer se rezultirajuće emisije sastoje od CO i određenih tvari, poput čađe (C), kao i pepela i drugih jednostavnih i složenih organskih spojeva. Dušikov oksid, ozon i aldehidi također se mogu stvoriti kao rezultat sekundarnih reakcija zbog prisutnosti drugih komponenata u zraku.
Ç8H18 (g) + 9/2 O.2 (g) → 8C (g) + 9 sati ujutro2O(1)
Napisala Jennifer Fogaça
Diplomirao kemiju
Brazilski školski tim
Želite li uputiti ovaj tekst u školskom ili akademskom radu? Izgled:
FOGAÇA, Jennifer Rocha Vargas. "Potpuno i nepotpuno izgaranje"; Brazil škola. Dostupno u: https://brasilescola.uol.com.br/quimica/combustao-completa-incompleta.htm. Pristupljeno 27. lipnja 2021.