Ponekad se može dogoditi da minimalna formula biti jednak molekulskoj formuli spoja; međutim, to nije uvijek istina.
Na primjer, empirijska ili minimalna formula za vodu je H2O, što ukazuje da postoji omjer 2: 1 između elemenata koji čine molekule vode. I, slučajno, ovo je također molekularna formula vode. Međutim, da biste se uvjerili da se to ne događa uvijek, pogledajte dva primjera u nastavku:
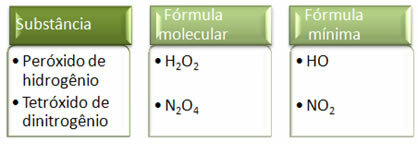
Budući da je minimalna formula samo omjer atoma svakog elementa, a ne stvarna količina njih u molekularnoj formuli, može se dogoditi različitih spojeva koji imaju istu empirijsku formulu, pa čak i minimalna formula spoja može biti ista kao i molekulska formula drugo. U primjeru u nastavku pogledajte kako se to može dogoditi:
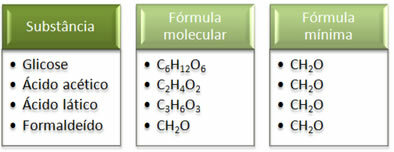
Vidi da je minimalna formula CH2Jednako je za sve tvari, tj. Ova minimalna formula izražava da, u svim slučajevima, atomi ugljika, vodika i kisika prisutni su u molekularnim formulama u omjeru 1:2:1. Nadalje, jedini koji ima istu molekulsku formulu kao i empirijska formula je formaldehid.
- Izračun minimalne ili empirijske formule:
Da bi se odredila empirijska formula spoja, prvo je potrebno znati koliki je njegov postotak ili približna formula. To se može učiniti mjerenjem mase svakog elementa u 100 g uzorka. Tekst "Postotak ili Centesimal Formula”Pojašnjava ovu stvar bolje.
Ne zaustavljaj se sada... Ima još toga nakon oglašavanja;)
Na primjer, recimo da je neposredni sastav datog spoja dan sa: 40,00% C, 6,67% H i 53,33% O. Te vrijednosti prenosimo u grame, uzimajući u obzir masu od 100 g složenog uzorka. Tako imamo: 40 g C, 6,67 g H i 53,33 g O.
Sada je potrebno te vrijednosti prenijeti na količinu materije (mol). To činimo dijeljenjem svake pronađene vrijednosti s njihovim molarnim masama:
C: 40/12 = 3,33
H: 6,67 / 1 = 6,67
O: 53,33 / 16 = 3,33
Budući da vrijednosti nisu cijeli brojevi, koristimo sljedeći uređaj: sve vrijednosti dijelimo s najmanjima, tako da se udio između njih ne mijenja.
U ovom je slučaju najmanja vrijednost 3,33, pa će rezultat biti:
C: 3,33 / 3,33 = 1
H: 6,67 / 3,33 = 2
O: 3,33 / 3,33 = 1
Dakle, minimalna formula ove nepoznate tvari jednaka je: Ç1H2O1 ili CH2O.
Ukratko, koraci potrebni za pronalaženje empirijske ili minimalne formule tvari su:

Napisala Jennifer Fogaça
Diplomirao kemiju
Želite li uputiti ovaj tekst u školskom ili akademskom radu? Izgled:
FOGAÇA, Jennifer Rocha Vargas. "Minimalna ili empirijska formula"; Brazil škola. Dostupno u: https://brasilescola.uol.com.br/quimica/formula-minima-ou-empirica.htm. Pristupljeno 28. lipnja 2021.