Tekst Prvi zakon radioaktivnosti ili Soddyev prvi zakon pokazao je prvi opći zakon koji odgovara onome što se događa kad atom radioaktivnog elementa prođe alfa raspadanje.
THE drugi zakon radioaktivnosti ili Soddyev drugi zakon odnosi se na beta propadanje. Pogledajte što kaže ovaj zakon:
“Kad atom emitira beta česticu, njegov atomski broj (Z) povećava se za jednu jedinicu, a maseni broj (A) ostaje isti. "
Općenito, ovaj zakon možemo predstaviti kroz sljedeću jednadžbu:
ZTHEx →-10β + Z + 1THEY
Atomski broj (Z) je broj protona u atomskoj jezgri. Masni broj (A) odgovara zbroju protona i neutrona u jezgri (A = p + n). To znači da je dobiveni atom izobare izvornog atoma, odnosno imaju isti maseni broj.
Evo primjera: torij-231 emitira beta česticu i stvara protaktin-231:
23190Th → -10β + 23191Pan
Imajte na umu da postoji očuvanje masenog broja i atomskog broja u dva člana jednadžbe:
A: 231 = 0 + 231;
Z: 90 = -1 + 91.
Dakle, pomoću ovog pravila možete saznati koja je čestica emitirana ili koji je atom nastao.
Kao što je objašnjeno u tekstu Beta izdanje (β), ova emisija je poput elektrona jer ima naboj -1 i nema masu. Ali zašto se onda atomski broj povećava, a maseni broj ostaje konstantan?
Ta je činjenica objašnjena hipotezom koju je pokrenuo talijanski fizičar Enrico Fermi (1901-1954).

Poštanska marka tiskana oko 2001. godine u SAD-u prikazuje sliku dobitnika Nobelove nagrade za fiziku Enrica Fermija
Ne zaustavljaj se sada... Ima još toga nakon oglašavanja;)
Enrico Fermi predložio je sljedeće:
“Emisija beta čestica događa se kada se nestabilni neutron unutar atomske jezgre raspadne, tvoreći proton koji ostaje u jezgri. U isto vrijeme ovaj raspad tvori beta česticu (-10β), koji je sličan elektronu i koji jezgra emitira zajedno s gama zračenje (γ - to je samo elektromagnetsko zračenje, bez električnog naboja ili mase) i neutrino (00ν, čestica naboja i nulta masa).”
Tj .:
01n → 11p + -10β + 00 γ + 00ν
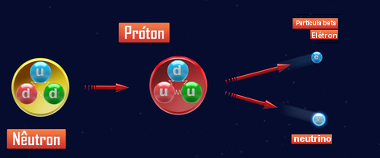
Raspad neutrona za emisiju beta čestica
Proton i neutron imaju praktički istu masu, zbog čega kada atom emitira beta česticu, njegov broj masa (A) ostaje ista, tj. dok se neutron raspada, proton nastaje zamjenjujući ga u jezgri, pa reći. Budući da nastaje proton, atomski broj se povećava za jedan.
Pogledajte sljedeću ilustraciju za još jedan primjer kako se ovaj zakon zapravo primjenjuje u slučajevima beta propadanja. U njemu izotop 14 elementa ugljik emitira beta česticu, pretvarajući se u dušik-14:

Beta raspadanje ugljika-14 koji stvara dušik-14
__________________
* Slika zaštićena autorskim pravima: modna pista / Shutterstock.com.
Napisala Jennifer Fogaça
Diplomirao kemiju
Želite li uputiti ovaj tekst u školskom ili akademskom radu? Izgled:
FOGAÇA, Jennifer Rocha Vargas. "Drugi zakon o radioaktivnosti ili Soddyev drugi zakon"; Brazil škola. Dostupno u: https://brasilescola.uol.com.br/quimica/segunda-lei-radioatividade-ou-segunda-lei-soddy.htm. Pristupljeno 27. lipnja 2021.