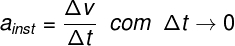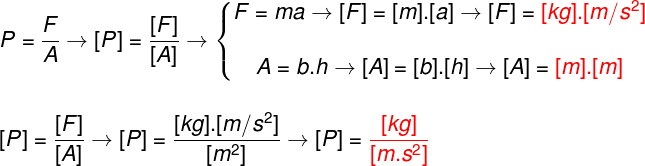ऊर्जाअंदर का का योग है गतिज ऊर्जा और एक शरीर के घटक परमाणुओं और अणुओं की गति से संबंधित क्षमता। आंतरिक ऊर्जा भी सीधे. के समानुपाती होती है तापमान शरीर का। यह एक अदिश राशि है जिसे जूल (SI) में मापा जाता है और चरों के फलन के रूप में निर्धारित किया जाता है जैसे कि दबाव (पी), आयतन (वी) और तापमान केल्विन (के) में एक प्रणाली के ऊष्मप्रवैगिकी (टी)।
किसी पिंड का तापमान जितना अधिक होता है, उसकी आंतरिक ऊर्जा उतनी ही अधिक होती है, इसलिए किसी कार्य को करने की उसकी क्षमता उतनी ही अधिक होती है। इसके अलावा, मोनोएटोमिक गैसों की आंतरिक ऊर्जा, उदाहरण के लिए, विशेष रूप से के योग द्वारा दी जाती है गतिज ऊर्जा गैस के प्रत्येक परमाणु का। आणविक गैसों, जैसे कि द्विपरमाणुक गैसों के साथ व्यवहार करते समय, आणविक अंतःक्रियाओं को ध्यान में रखना चाहिए और, के लिए यह, आंतरिक ऊर्जा अणुओं की गतिज ऊर्जा के योग के बीच मौजूद संभावित ऊर्जा के साथ निर्धारित होती है वे।
अब मत रोको... विज्ञापन के बाद और भी बहुत कुछ है;)
आदर्श एकपरमाणुक गैसों की आंतरिक ऊर्जा
चूंकि एक आदर्श एकपरमाणुक गैस के परमाणुओं के बीच कोई अंतःक्रिया नहीं होती है, इसकी आंतरिक ऊर्जा विशेष रूप से दो चरों पर निर्भर करती है: मोल्स की संख्या (एन) और गैस तापमान (टी)। घड़ी:
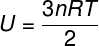
यू - आंतरिक ऊर्जा
नहीं न - मोल्स की संख्या
आर - उत्तम गैसों का सार्वत्रिक नियतांक
टी - तापमान
उपरोक्त समीकरण में, आर इसमें 0.082 एटीएम का मापांक है। एल / मोल। के या 8.31 जे/मोल। के (एसआई)। इसके अलावा, हम उपरोक्त समीकरण को अन्य मात्राओं, जैसे दबाव और आयतन के रूप में भी लिख सकते हैं। उसके लिए, हमें याद रखने की जरूरत है क्लैपेरॉन का समीकरण, आदर्श गैसों के लिए उपयोग किया जाता है।
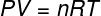
पिछले समीकरण के लिए उपरोक्त समीकरण को प्रतिस्थापित करने पर, हमारे पास आंतरिक ऊर्जा की गणना के लिए निम्नलिखित अभिव्यक्ति होगी:
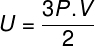
नज़रयह भी:एक आदर्श गैस क्या है?
उपरोक्त समीकरणों को ध्यान में रखते हुए, एक आदर्श मोनोएटोमिक गैस के परमाणुओं की गतिज ऊर्जा और उसके तापमान के बीच संबंध निर्धारित करना संभव है। इसके लिए हम बताएंगे कि इस प्रकार की गैस की गतिज ऊर्जा है विशुद्ध रूप सेगतिकी। घड़ी:
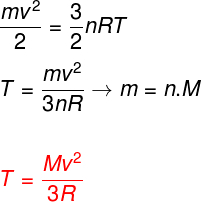
म - पास्ता
नहीं न - तिल संख्या
म - अणु भार
कई स्थितियों में, यह जानना दिलचस्प है कि गैस की आंतरिक ऊर्जा (ΔU) की भिन्नता की गणना कैसे की जाती है, क्योंकि यह मात्रा इंगित करती है कि गैस प्राप्त हो गया है या छोड़ दिया ऊर्जा। यदि गैस की आंतरिक ऊर्जा का परिवर्तन धनात्मक (ΔU > 0) रहा हो, तो गैस को ऊर्जा प्राप्त होगी; अन्यथा (ΔU< 0), गैस ने अपनी ऊर्जा का कुछ भाग छोड़ दिया होगा।
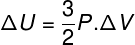
गैस आयतन भिन्नता के संदर्भ में आंतरिक ऊर्जा भिन्नता।
द्विपरमाणुक गैसों के लिए आंतरिक ऊर्जा
आदर्श द्विपरमाणुक गैसों के लिए, आंतरिक ऊर्जा थोड़ी भिन्न समीकरण द्वारा दी जाती है।
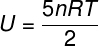
थर्मोडायनामिक परिवर्तनों और चक्रों में आंतरिक ऊर्जा
के अनुसार ऊष्मप्रवैगिकी का पहला नियम, एक आदर्श गैस की आंतरिक ऊर्जा निश्चित रूप से भिन्न हो सकती है ऊष्मप्रवैगिकी परिवर्तन, परिवेश और सिस्टम के बीच आदान-प्रदान की गई गर्मी की मात्रा के साथ-साथ सिस्टम द्वारा या उस पर किए गए कार्य के आधार पर।
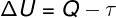
क्यू - तपिश
τ - काम क
इसके बाद, आइए कुछ विशेष उष्मागतिकी परिवर्तनों के लिए इस नियम के स्वरूप को देखें।
नज़रयह भी:थर्मल मशीनों का इतिहास
→ आंतरिक ऊर्जा: समतापीय परिवर्तन
पर समतापी परिवर्तन, कोई तापमान परिवर्तन नहीं होता है और इसलिए आंतरिक ऊर्जा स्थिर रहती है।
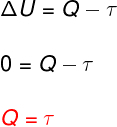
इस मामले में, सिस्टम के साथ आदान-प्रदान की जाने वाली गर्मी की पूरी मात्रा काम में बदल जाती है और इसके विपरीत।
→ आंतरिक ऊर्जा: आइसोवोल्यूमेट्रिक परिवर्तन
पर आइसोवॉल्यूमेट्रिक ट्रांसफॉर्मेशन, कार्य करना संभव नहीं है, क्योंकि सिस्टम एक कठोर और विस्तार योग्य कंटेनर में सीमित है। इस मामले में, सिस्टम के साथ आदान-प्रदान की जाने वाली गर्मी की पूरी मात्रा सीधे इसकी आंतरिक ऊर्जा को बदलती है।
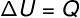
→ आंतरिक ऊर्जा: समदाब रेखीय परिवर्तन
इस प्रकार के परिवर्तन में, प्रणाली के अधीन है a निरंतर दबावइसलिए, उसके द्वारा या उस पर किए गए कार्य की गणना विश्लेषणात्मक रूप से की जा सकती है।
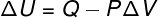
→ आंतरिक ऊर्जा: रुद्धोष्म परिवर्तन
में रुद्धोष्म परिवर्तनसिस्टम और उसके परिवेश के बीच कोई हीट एक्सचेंज नहीं होता है, इसलिए आंतरिक ऊर्जा की भिन्नता केवल सिस्टम द्वारा या उसके द्वारा किए गए कार्य पर निर्भर करती है।
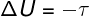
चक्रीय प्रक्रियाओं में आंतरिक ऊर्जा
प्रत्येक चक्रीय प्रक्रिया में, एक प्रणाली की थर्मोडायनामिक अवस्था, जो उसके दबाव, आयतन और तापमान चर (P, V, T) द्वारा दर्शायी जाती है, है परिवर्तित हो जाता है, लेकिन मूल अवस्था (P, V, T) में लौट आता है, इसलिए, इस प्रकार की प्रक्रिया में आंतरिक ऊर्जा की भिन्नता हमेशा शून्य होती है (ΔU = 0).
नज़रयह भी:चक्रीय परिवर्तन
नीचे दिए गए ग्राफ को देखें, जो राज्यों ए और बी के बीच तीन अलग-अलग थर्मोडायनामिक परिवर्तनों को दर्शाता है।
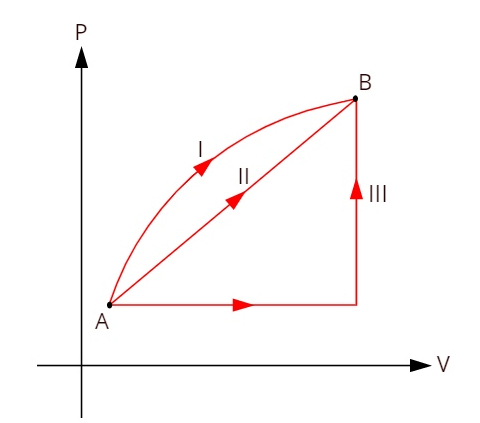
चूंकि तीन परिवर्तन (I, II और III) राज्य A को छोड़ कर राज्य B में जाते हैं, आंतरिक ऊर्जा भिन्नता उन सभी के लिए समान होनी चाहिए, इसलिए:
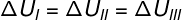
आंतरिक ऊर्जा व्यायाम
1) एक आदर्श द्विपरमाणुक गैस के दो मोल, जिसका दाढ़ द्रव्यमान 24 g/mol के बराबर है, 500 K के तापमान पर एक बंद, कठोर कंटेनर के अंदर पाए जाते हैं, जिसका आयतन 10-3 एम³ निर्धारित करें:
ए) जूल में इस गैस की आंतरिक ऊर्जा का मापांक।
b) वह दबाव जो गैस कंटेनर की दीवारों पर डालती है।
संकल्प:
द) चूंकि यह एक आदर्श और द्विपरमाणुक गैस है, हम इसकी आंतरिक ऊर्जा की गणना के लिए नीचे दिए गए सूत्र का उपयोग करेंगे:
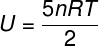
अभ्यास विवरण में सूचित किए गए डेटा को लेते हुए, हमारे पास हल करने के लिए निम्नलिखित गणना होगी:
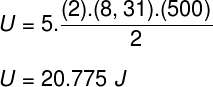
बी) हम उस दबाव को निर्धारित कर सकते हैं जो गैस एक बार उसके कंटेनर की मात्रा जानने के बाद डालती है: 10-3 एम³ ऐसा करने के लिए, हम निम्नलिखित सूत्र का उपयोग करेंगे:
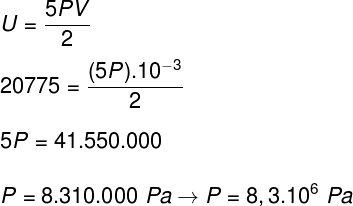
मेरे द्वारा राफेल हेलरब्रॉक