चूँकि अष्टक नियम के अपवाद हैं, हम अणु बनाने में परमाणुओं के बीच सही व्यवस्था कैसे जान सकते हैं?
यह प्रत्येक संरचना के औपचारिक भार की गणना करके किया जा सकता है। औपचारिक शुल्क जो शून्य के सबसे करीब है, वह वास्तविक अस्तित्व की सबसे बड़ी संभावना वाला होगा। ध्यान दें कि यह "शून्य के सबसे करीब" है, इसलिए इसका शून्य होना जरूरी नहीं है।
औपचारिक प्रभार सूत्र (सी .)एफओ) é:
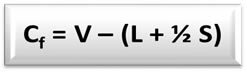
वी = मुक्त परमाणु के वैलेंस इलेक्ट्रॉनों की संख्या;
एल = संरचना में परमाणु के पृथक (गैर-बंधन) जोड़े में मौजूद इलेक्ट्रॉनों की संख्या;
एस = संरचना में परमाणु द्वारा साझा किए गए इलेक्ट्रॉनों की संख्या।
यह कैसे होता है यह समझने के लिए, कल्पना कीजिए कि हम जानना चाहते हैं कि SO अणु के लिए लुईस इलेक्ट्रॉनिक संरचना क्या है।2. हमारे पास परमाणुओं के बीच दो संभावित व्यवस्थाएँ हैं:
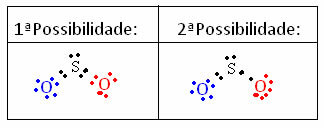
संरचनाओं में भाग लेने वाले सभी परमाणुओं के औपचारिक प्रभार की गणना की जाती है। देखो:
पहली संभावना:
सल्फर (एस): ऑक्सीजन (ओ) ऑक्सीजन (ओ)
सीच (एस) = 6 – (2 + ½ 8) सीच (एस) = 6 – (4 + ½ 4) सीच (एस) = 6 – (4 + ½ 4)
सीच (एस) =0 सीच (एस) =0 सीच (एस) =0
अब मत रोको... विज्ञापन के बाद और भी बहुत कुछ है;)
दूसरी संभावना:
सल्फर (एस): ऑक्सीजन (ओ) ऑक्सीजन (ओ)
सीच (एस) = 6 – (2 + ½ 6) सीच (एस) = 6 – (6 + ½ 2) सीच (एस) = 6 – (4 + ½ 4)
सीच (एस) = +1सीच (एस) = -1 सीच (एस) =0
प्राप्त परिणामों के आधार पर, हम ध्यान दे सकते हैं कि पहली संरचना वास्तविक अस्तित्व की उच्चतम संभावना वाली संरचना है। तो, हम जानते हैं कि यह ऑक्टेट नियम का पालन नहीं करता है, लेकिन सल्फर ने अपने वैलेंस शेल का विस्तार किया है, 10 इलेक्ट्रॉनों के साथ स्थिर रहता है।
यह नियम सही आयन व्यवस्था खोजने पर भी लागू होता है।
जेनिफर फोगाका द्वारा
रसायन विज्ञान में स्नातक
क्या आप इस पाठ को किसी स्कूल या शैक्षणिक कार्य में संदर्भित करना चाहेंगे? देखो:
FOGAÇA, जेनिफर रोचा वर्गास। "औपचारिक लोड गणना"; ब्राजील स्कूल. में उपलब्ध: https://brasilescola.uol.com.br/quimica/calculo-carga-formal.htm. 28 जून, 2021 को एक्सेस किया गया।


