क्लैपेरॉन समीकरण एक गणितीय व्यंजक है जो मात्राओं से संबंधित है जैसे कि दबाव (पी), आयतन (वी), तापमान (टी) और कणों की संख्या (एन) जो ए. बनाते हैं सही या आदर्श गैस. इस समीकरण का नाम फ्रांसीसी भौतिक विज्ञानी के नाम पर रखा गया है पॉलएमिलक्लैपेरॉन और के अनुभवजन्य कानूनों के सामान्यीकरण के रूप में समझा जा सकता है गैसोंउत्तममेंगे-लुसाक, चार्ल्स और बॉयल। यह आदर्श गैसों के अध्ययन के लिए मौलिक था और के विकास को सक्षम बनाता था थर्मल मशीन, पिछले कुछ दशकों में उन्हें अधिक से अधिक कुशल बना रहा है।
यह भी देखें: दुर्घटना से हुई भौतिकी की खोज
क्लैपेरॉन का समीकरण: आदर्श गैस कानून
क्लैपेरॉन का समीकरण है तीन अनुभवजन्य कानूनों से व्युत्पन्न, यानी ऐसे कानून जो प्रयोगों से निर्धारित किए गए थे. इस तरह के कानून गैसों के व्यवहार की व्याख्या करते हैं गैस परिवर्तनआइसोवॉल्यूमेट्रिक (गे-लुसाक कानून), समदाब रेखीय (चार्ल्स लॉ) और समतापी (बाॅय्ल का नियम)। इन कानूनों के अनुसार:
परिवर्तनों में आइसोवॉल्यूमेट्रिक, एक आदर्श गैस के दबाव और थर्मोडायनामिक तापमान के बीच का अनुपात स्थिर रहता है;
परिवर्तनों में समदाब रेखीय, एक आदर्श गैस के आयतन और थर्मोडायनामिक तापमान के बीच का अनुपात स्थिर होता है;
- परिवर्तनों में समतापी, एक आदर्श गैस के दबाव और आयतन का गुणनफल स्थिर रहता है।
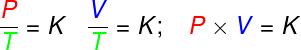
पी - दबाव (पीए - पास्कल)
वी - गैस की मात्रा (एम³)
टी - थर्मोडायनामिक गैस तापमान (के - केल्विन)
उपरोक्त तीन कानूनों से, क्लैपेरॉन समीकरण निर्धारित करता है कि इसका मूल्य क्या है लगातार (क) उपर्युक्त परिवर्तनों में से प्रत्येक में प्राप्त किया। क्लैपेरॉन के समीकरण के अनुसार, यह स्थिरांक मोलों की संख्या को a by से गुणा करने के बराबर है निरंतर आर, आदर्श गैसों के सार्वत्रिक स्थिरांक के रूप में जाना जाता है, और बराबर बोल्ट्जमान स्थिरांक से गुणा अवोगाद्रो की संख्या.
सूत्र
उस सूत्र की जाँच करें जिसे के रूप में जाना जाता है समीकरणमेंक्लैपेरॉन:
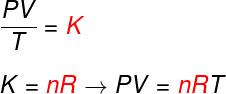
नहीं न - मोल्स की संख्या (mol)
आर - आदर्श गैसों का सार्वत्रिक स्थिरांक (R = 0.082 atm.l/mol. के या 8.314 जे.मोल/के)
क्लैपेरॉन समीकरण का विश्लेषण करते हुए, यह देखना संभव है कि दबाव आदर्श गैसों द्वारा उत्सर्जित होता है तापमान के सीधे आनुपातिक और करने के लिए भी मोल्स की संख्या. इसके अलावा, दाब आयतन के व्युत्क्रमानुपाती होता है गैस द्वारा कब्जा कर लिया।
हे आदर्श गैस मॉडल क्लैपेरॉन समीकरण द्वारा संभव बनाया गया है जिसका व्यापक रूप से उपयोग किया जाता है द्वारा संचालित मशीनों का विकास तरल पदार्थ, जैसे भाप से चलने वाली मशीनें और आंतरिक दहन इंजन।
क्लैपेरॉन समीकरण से कई महत्वपूर्ण परिणाम प्राप्त किए जा सकते हैं। उनमें से एक, उदाहरण के लिए, भविष्यवाणी करता है कि किसी भी आदर्श गैस के 1 मोल का आयतन होता है 22.4 एल जब के दबाव के अधीन 1 एटीएम (1,01.105 पा) और के तापमान पर 273K (0 डिग्री सेल्सियस)।
यह भी देखें: थर्मोलॉजी में सबसे महत्वपूर्ण अवधारणाएं
क्लैपेरॉन समीकरण पर हल किए गए अभ्यास
प्रश्न १ —(यूईसीई) एक गैस जिसका तापमान, आयतन और दबाव PV = nRT से संबंधित हो सकता है, में निम्नलिखित विशेषताएं हैं:
ए) अणुओं के बीच बहुत बड़ी औसत दूरी, जब टकराने के अलावा, इंटरमॉलिक्युलर इंटरैक्शन की अवहेलना करने के लिए; अणु लोचदार टकराव से गुजरते हैं।
बी) अणुओं के बीच बहुत कम औसत दूरी; अणु लोचदार टकराव से गुजरते हैं।
ग) अणुओं के बीच बहुत बड़ी औसत दूरी, जब टकराने को छोड़कर, अंतर-आणविक अंतःक्रियाओं की अवहेलना करने के लिए; अणु लोचदार टकराव से गुजरते हैं।
घ) अणुओं के बीच और मजबूत अंतर-आणविक अंतःक्रियाओं के साथ बहुत बड़ी औसत दूरी; अणु लोचदार टकराव से गुजरते हैं।
संकल्प:
आदर्श गैस मॉडल में, बड़ी संख्या में आयामहीन कण यादृच्छिक दिशाओं में उच्च गति से चलते हैं। इन कणों द्वारा झेली गई एकमात्र बातचीत पूरी तरह से लोचदार टकराव है, इसलिए सही विकल्प है एक पत्र.
प्रश्न २ —(यूएफआरजीएस) आदर्श गैसों के बारे में निम्नलिखित कथनों पर विचार करें।
मैं। गैसों pV = nRT के लिए राज्य के समीकरण में मौजूद स्थिरांक R का मान सभी आदर्श गैसों के लिए समान होता है।
द्वितीय. समान ताप और दाब पर विभिन्न आदर्श गैसों के समान आयतन में अणुओं की संख्या समान होती है।
III. एक आदर्श गैस के अणुओं की औसत गतिज ऊर्जा गैस के निरपेक्ष तापमान के सीधे आनुपातिक होती है।
कौन से सही हैं?
ए) केवल मैं
बी) केवल II
ग) केवल III
d) केवल I और II
ई) मैं, द्वितीय और तृतीय
खाका:
आइए विकल्पों को देखें:
मैं। सही बात, इसलिए इसे आदर्श गैसों का सार्वत्रिक नियतांक कहते हैं।
द्वितीय. सही बात. क्लैपेरॉन के समीकरण के अनुसार, यदि दो आदर्श गैसों का दबाव, तापमान और आयतन समान हो, तो उन गैसों में कणों की संख्या बराबर होती है।
III. सही बात. ऊर्जा समविभाजन प्रमेय के अनुसार, एक आदर्श गैस में कणों की गतिज ऊर्जा उसके तापमान के समानुपाती होती है।
अतः सही विकल्प है पत्र ई.
प्रश्न 3 - (यूएफजेएफक्लैपेरॉन, बॉयल, मैरियट, गे-लुसाक, वैन डेर वॉल्स जैसे पुरुषों ने गैसों के गुणों से संबंधित महत्वपूर्ण अध्ययन विकसित किए हैं। वास्तविक गैसों का व्यवहार कम दबाव की स्थिति में आदर्श गैसों के साथ-साथ बड़ी मात्रा में निहित गैसों और उच्च तापमान पर मौजूद गैसों के समान होता है। मान लीजिए कि, एक प्रयोगशाला प्रयोग में, वॉल्यूम V का एक कंटेनर पूरी तरह से बंद है और इसमें 4.0 के दबाव में एक आदर्श गैस का 1 मोल है। atm 127 º C के बराबर तापमान पर विस्तार के अधीन है और यह कि इस गैस का व्यवहार एक आदर्श गैस जैसा है, जैसा कि दिखाया गया है ग्राफिक।
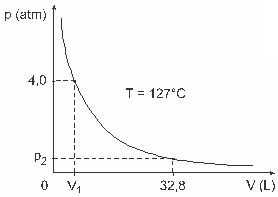
इस स्थिति में, जब गैस 32.8 L के बराबर आयतन ग्रहण कर रही हो, तो इसके द्वारा लगाया जाने वाला दबाव होगा:
(दिया गया है: पूर्ण गैसों का सार्वत्रिक नियतांक R = 0.082 atm है। एल / मोल। क।)
ए) 0.32 एटीएम
बी) 0.40 एटीएम
सी) 1.0 एटीएम
डी) 2.0 एटीएम
ई) 2.6 एटीएम
संकल्प:
पत्र सी.
अभ्यास को हल करने के लिए, हमें डेटा को क्लैपेरॉन समीकरण में लागू करने की आवश्यकता है, लेकिन इससे पहले हमें तापमान, जो डिग्री सेल्सियस में है, को केल्विन में बदलने की आवश्यकता है। चेक आउट:

राफेल हेलरबॉक द्वारा
भौतिक विज्ञान के अध्यापक
स्रोत: ब्राजील स्कूल - https://brasilescola.uol.com.br/fisica/a-equacao-clapeyron.htm
