आप धातुओं वे रासायनिक तत्व हैं जो अपनी मुख्य भौतिक विशेषता के रूप में इलेक्ट्रॉनों को खोने की क्षमता के रूप में उपस्थित होते हैं और परिणामस्वरूप, धातु के धनायन बनाते हैं। इस कारण से, वे दो प्रकार के रासायनिक बंधन बना सकते हैं: आयनिक बंधन और and धात्विक बंधन.
आयोनिक बंध तब होता है जब कोई धातु धात्विक प्रकृति के एक तत्व के साथ परस्पर क्रिया करता है, जो हो सकता है a अधातु या हाइड्रोजन। इस प्रकार के बंधन में, हमें धातुओं द्वारा इलेक्ट्रॉनों की हानि और अधातुओं या हाइड्रोजन द्वारा इलेक्ट्रॉनों की प्राप्ति होती है।
पहले से ही धात्विक बंधन एक धातु तत्व के परमाणुओं के बीच स्थापित होता है। इस प्रकार का बंधन केवल एक धातु के परमाणुओं के बीच होता है और विशेष रूप से क्योंकि एक धातु किसी अन्य धातु तत्व के साथ रासायनिक बंधन स्थापित नहीं कर सकता है।
धातुओं की सामान्य विशेषताएं
पारा के अपवाद के साथ, कमरे के तापमान पर ठोस;
वे शानदार हैं;
उनके उच्च गलनांक और क्वथनांक होते हैं;
वे आम तौर पर चांदी के रंग के होते हैं, सोने के अपवाद के साथ, जो सुनहरा होता है, और तांबा, जो लाल रंग का होता है;
शुद्ध धातुएं परमाणुओं के समूहों (एक रासायनिक तत्व के) से बनती हैं जिन्हें क्रिस्टल जाली कहा जाता है।
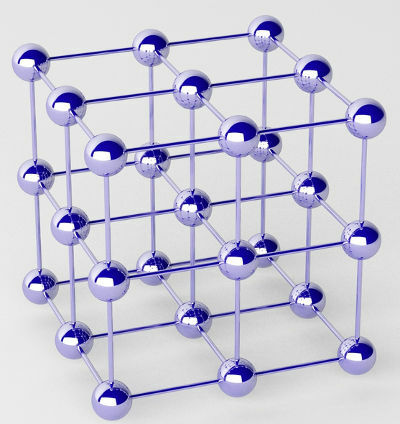
किसी धातु के क्रिस्टलीय जालक का निरूपण
धातु बंधन के सिद्धांत bond
पर धात्विक बंधन, धातु बनाने वाले क्रिस्टलीय जाली वास्तव में एक आयनिक क्लस्टर होते हैं (केवल से बना होता है) फैटायनों और इलेक्ट्रॉन)। धातु के परमाणुओं की संयोजकता परत में मौजूद इलेक्ट्रॉनों को स्थानीयकृत किया जाता है, अर्थात वे संयोजकता परत को छोड़ देते हैं, जिससे परमाणु एक धनायन (इलेक्ट्रॉनों में कमी) बन जाता है।
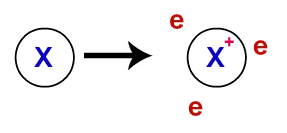
संयोजकता कोश से निरूपित इलेक्ट्रॉनों का निरूपण
निरूपित होने के बाद, धातु के परमाणुओं से इलेक्ट्रॉन एक सच्चे "इलेक्ट्रॉन समुद्र" का निर्माण करते हुए, धनायनों को घेरने लगते हैं। इस समुद्र में मौजूद प्रत्येक इलेक्ट्रॉन में धातु के क्रिस्टलीय जाली के माध्यम से स्वतंत्र रूप से घूमने की क्षमता होती है।

इलेक्ट्रॉन समुद्री मॉडल का प्रतिनिधित्व
ध्यान दें: इलेक्ट्रॉन "समुद्र से" क्रिस्टल जाली को छोड़ने और इसके माध्यम से आगे बढ़ने में सक्षम नहीं हैं।
धात्विक बंधन द्वारा उचित धातुओं के गुण
ए) लचीलापन
एक धातु के माध्यम से, विभिन्न मोटाई और चादरों की चादरें बनाना संभव है। धातुओं के इस गुण के कारण ही हम विभिन्न वस्तुओं का निर्माण कर सकते हैं, जैसे चाकू, तलवार आदि।

तलवार का ब्लेड धातु से बना होता है
बी) चालकता
धातुएँ सामान्यतः विद्युत धारा और ऊष्मा की सुचालक होती हैं। जब कोई धातु ऊष्मा स्रोत या विद्युत प्रवाह के स्रोत के संपर्क में होती है, तो वह उन्हें संचालित करने में सक्षम होती है।

एक स्टोव की लौ में एक एल्यूमीनियम पैन चालकता के कारण पूरी तरह से गर्म हो जाता है।
सी) लचीलापन
एक धातु के माध्यम से, हम तारों का उत्पादन कर सकते हैं। तारों के रूप में धातु का उपयोग इसके उपयोग को सुविधाजनक बनाता है, विशेष रूप से विद्युत चालकता के संबंध में।

तांबे जैसी धातु का उपयोग तार बनाने के लिए किया जा सकता है।
मेरे द्वारा। डिओगो लोपेज डायस
स्रोत: ब्राजील स्कूल - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-ligacao-metalica.htm

