एसपी-प्रकार कार्बन संकरण यह तभी होता है जब यह दो पाई बंध (π) और दो सिग्मा बंध (σ) बनाता है। इस मामले में, दो संभावनाएं हैं: कार्बन दो डबल बॉन्ड या सिंगल और ट्रिपल बॉन्ड बना सकता है, जैसा कि नीचे दिखाया गया है:
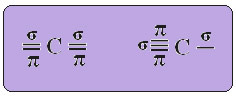
ये पाठ "सपा प्रकार संकरण3” विस्तार से दिखाता है कि कार्बन संकरण कैसे होता है। याद रखना: संकरण शुद्ध परमाणु ऑर्बिटल्स का "मिश्रण" है, जो एक दूसरे के समतुल्य हाइब्रिड परमाणु ऑर्बिटल्स की उत्पत्ति करते हैं, लेकिन मूल शुद्ध ऑर्बिटल्स से अलग होते हैं। तो, यह कार्बन ऑर्बिटल्स में होता है जिन्हें मूल रूप से इस तरह दर्शाया गया था:
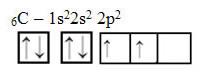
हालांकि, ऊर्जा की प्राप्ति के साथ, 2s कक्षीय से एक इलेक्ट्रॉन (एक तीर द्वारा दर्शाया गया) को 2p कक्षीय में पदोन्नत किया जाता है:
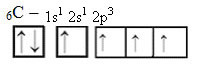
इस तरह, कार्बन के चार अयुग्मित कक्षक हैं, जो केवल दो नहीं, बल्कि चार सहसंयोजक बंधन बनाने में सक्षम हैं।
एसपी-प्रकार के संकरण के मामले में, हम जानते हैं कि दो बांड पीआई होंगे; ये शुद्ध "पी" ऑर्बिटल्स में होते हैं, जबकि अन्य दो ऑर्बिटल्स, जो कि एसपी हाइब्रिड हैं, शेष सिग्मा बॉन्ड बनाएंगे।
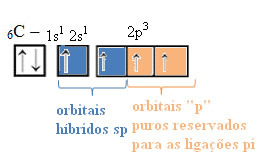
एक एस और एपी कक्षीय के बीच इस संकरण का स्थानिक प्रतिनिधित्व, एक संकर एसपी कक्षीय को जन्म देता है, जिसे निम्नानुसार दर्शाया जा सकता है:
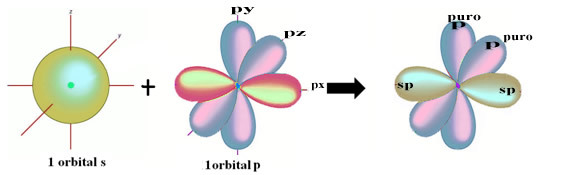
ऊपर की आकृति में यह बहुत स्पष्ट है कि दो शुद्ध कक्षाएँ हैं जो पाई बंध बनाती हैं।
यह कैसे होता है, इसे समझने के लिए, आइए एक उदाहरण के रूप में साइनाइड गैस (एचसीएन) के एक अणु को लें, जिसका इस्तेमाल संयुक्त राज्य अमेरिका में मौत की सजा वाले कैदियों के लिए गैस कक्षों में किया जाता है। इसका संरचनात्मक सूत्र द्वारा दिया गया है:
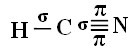
कार्बन के लिए, इसके परमाणु कक्षक पहले ही दिखाए जा चुके हैं, अब हाइड्रोजन और नाइट्रोजन कक्षकों को देखें:
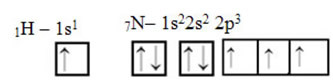
ध्यान दें कि अयुग्मित हाइड्रोजन ऑर्बिटल जो सिग्मा बॉन्ड का प्रदर्शन करेगा, वह "s" है, जिसे स्थानिक रूप से एक सर्कल द्वारा दर्शाया जाता है; और नाइट्रोजन ऑर्बिटल्स "पी" प्रकार के होते हैं, जिन्हें तीन डबल ओवोइड्स (प्रत्येक एक स्थानिक क्षेत्र में: x, y, z) द्वारा दर्शाया जाता है। इस प्रकार, एचसीएन अणु की संरचना को निम्नानुसार दर्शाया गया है:
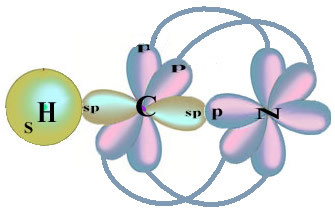
इस फॉर्मलाडेहाइड संरचना में मौजूद बांडों के प्रकार के लिए, हमारे पास है:
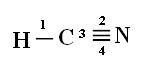
सम्बन्ध: 1 = σएस-एसपी
2 = σपी-एसपी
3 = 4 = πपी-पी
जेनिफर फोगाका द्वारा
रसायन विज्ञान में स्नातक
स्रोत: ब्राजील स्कूल - https://brasilescola.uol.com.br/quimica/hibridizacao-tipo-sp.htm
