ए की ताकत का अध्ययन अम्ल विद्युत प्रवाह के संचालन के लिए अम्लीय घोल की क्षमता निर्धारित करने के लिए बहुत महत्वपूर्ण है, क्योंकि यह उन आयनों की मात्रा से संबंधित है जो यह पदार्थ पानी के संपर्क में आने पर पैदा करता है (आयनीकरण). जब कोई अम्ल बहुत अधिक प्रबल होता है, तो वह बहुत अधिक हाइड्रोनियम धनायन (H .) उत्पन्न करता है3हे+) और कई आयन (X .)-). हाइड्रोब्रोमिक एसिड आयनीकरण समीकरण देखें:
एचबीआर + एच2ओ → एच3हे+ + भाई-
आयनीकरण करते समय, एसिड अणु में मौजूद हाइड्रोजन पानी के अणु के साथ संपर्क करता है और हाइड्रोनियम बनाता है। लेकिन इस घटना के घटित होने के लिए, हाइड्रोजन परमाणु का आयनीकरण होना आवश्यक है। आयनीकृत हाइड्रोजन वह है जो हाइड्रोनियम धनायन बनाने में सक्षम है।. यह पता लगाने के लिए कि क्या हाइड्रोजन आयनीकरण योग्य है, हम एसिड के वर्गीकरण को हाइड्रासिड (इसकी संरचना में कोई ऑक्सीजन नहीं है) या ऑक्सीएसिड (इसकी संरचना में ऑक्सीजन है) के रूप में लेते हैं।
ए) हिड्रासिड्स
एक हाइड्रासिड में सभी हाइड्रोजन को आयनीकरण योग्य माना जाता है।
उदाहरण:
- एचसीएल: एक आयनीकरण योग्य हाइड्रोजन, इस प्रकार एक हाइड्रोनियम का उत्पादन;
- हो2एस: दो आयनीकरण योग्य हाइड्रोजन, इसलिए दो हाइड्रोन उत्पन्न करें
बी) ऑक्सीएसिड
एक ऑक्सीएसिड में, केवल हाइड्रोजन जो अणु में ऑक्सीजन परमाणु से बंधी होती है, उसे आयनित करने योग्य माना जाता है। इसके लिए जरूरी है कि इसका स्ट्रक्चरल फॉर्मूला तैयार किया जाए। कुछ उदाहरण देखें:
एच3धूल4 (फॉस्फोरिक एसिड)
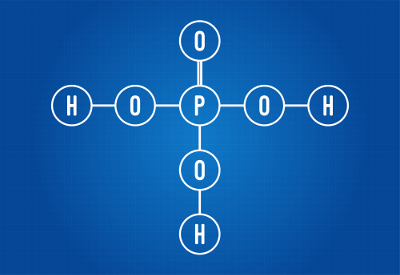
फॉस्फोरिक एसिड का संरचनात्मक सूत्र
हम देख सकते हैं कि, फॉस्फोरिक एसिड की संरचना में, ऑक्सीजन से बंधे तीन हाइड्रोजन होते हैं, इसलिए तीन आयनीकरण योग्य हाइड्रोजन होते हैं। आयनीकरण समीकरण होगा:
एच3धूल4 + 3 एच2ओ → 3 एच3हे+ + पीओ4-3
एच2केवल4 (सल्फ्यूरिक एसिड)
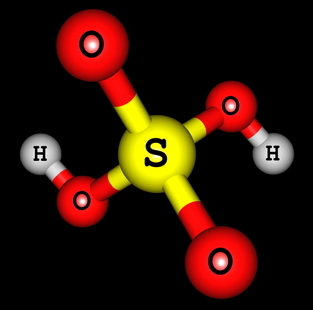
सल्फ्यूरिक एसिड का संरचनात्मक सूत्र
हम देख सकते हैं कि, सल्फ्यूरिक एसिड की संरचना में, दो हाइड्रोजन ऑक्सीजन से बंधे होते हैं, इसलिए दो आयनीकरण योग्य हाइड्रोजन होते हैं। आयनीकरण समीकरण होगा:
एच2केवल4 + 2 एच2ओ → 2 एच3हे+ + ओएस4-2
मेरे द्वारा। डिओगो लोपेज डायस
स्रोत: ब्राजील स्कूल - https://brasilescola.uol.com.br/quimica/hidrogenios-ionizaveis.htm
