निहोनियम, परमाणु संख्या 113 और प्रतीक एनएच, आवर्त सारणी के समूह 13 से संबंधित एक रासायनिक तत्व है। इसके अलावा, यह प्रकृति में नहीं पाया जाने वाला एक अति-भारी तत्व है। इस प्रकार, इसकी प्राप्ति केवल कृत्रिम रूप से, परमाणु संलयन प्रतिक्रियाओं के माध्यम से की जा सकती है। निहोनियम की रासायनिक विशेषताएं अभी भी इतनी स्पष्ट नहीं हैं, लेकिन यह अनुमान लगाया जाता है कि यह कुछ मामलों में अपने हल्के समकक्ष, थैलियम के समान व्यवहार करता है।
निहोनियम शुरू में पिघलने से प्राप्त किया गया था 70Zn के साथ 209बीआई, 2003 में रिकेन इंस्टीट्यूट, जापान में। यद्यपि रूसी और अमेरिकी वैज्ञानिकों ने भी तत्व 113 के खोजकर्ताओं के रूप में पहचाने जाने के लिए कहा, आईयूपीएसी ने जापानी वैज्ञानिकों को मान्यता दी। नाम निहोन शब्द को संदर्भित करता है, क्योंकि जापानी अपने मूल देश को बुलाते हैं।
यह भी पढ़ें: गैलियम - आवर्त सारणी के समूह 13 से संबंधित एक अन्य रासायनिक तत्व
निहोनियम के बारे में सारांश
यह एक सिंथेटिक रासायनिक तत्व है जो के समूह 13 में स्थित है आवर्त सारणी.
इसका उत्पादन 2003 में जापान के रिकेन इंस्टीट्यूट में शुरू हुआ था।
यह 2015 में आवर्त सारणी में हाल ही में शामिल किए गए तत्वों का समूह बनाता है।
उनके अध्ययन अभी भी बहुत हाल के हैं, लेकिन कुछ लोग इसे समूह 13 के अन्य तत्वों जैसे कि थैलियम से जोड़ना चाहते हैं।
इसका उत्पादन है परमाणु संलयन, के समस्थानिकों का उपयोग करना 70Zn और के परमाणु 209द्वि.
निहोनियम गुण
प्रतीक: नाह
परमाणु संख्या: 113
परमाणु भार: 278 और 286 cu के बीच (Iupac द्वारा अनौपचारिक)
इलेक्ट्रोनिक विन्यास: [आरएन] 7s2 5f14 6डी10 7p1
सबसे स्थिर आइसोटोप:286एनएच (9.5 सेकंड .) हाफ लाइफ, जो 6.3 सेकंड तक बढ़ सकता है या 2.7 सेकंड कम हो सकता है)
रासायनिक श्रृंखला: समूह 13, अत्यधिक भारी तत्व
निहोनियम की विशेषताएं
निहोनियम, प्रतीक एनएच और परमाणु संख्या 113, आवर्त सारणी में शामिल अंतिम तत्वों में से एक था. इसका आधिकारिककरण 30 दिसंबर, 2015 को इंटरनेशनल यूनियन ऑफ प्योर एंड एप्लाइड केमिस्ट्री (IUPAC) द्वारा किया गया था, जबकि इसका नाम केवल 2016 के मध्य में ही आधिकारिक किया गया था।
आवर्त सारणी के इस क्षेत्र के तत्व अत्यधिक अस्थिर हैं, अर्थात वे प्रकृति में नहीं पाए जा सकते हैं। इस प्रकार, एक कथित अस्तित्व के सामने, वे लगभग तुरंत रेडियोधर्मी क्षय से गुजरेंगे - परमाणु कणों का उत्सर्जन, जैसे कि α और β - अधिक स्थिरता प्राप्त करने के लिए।
हालाँकि, जब वे परमाणु कणों का उत्सर्जन करते हैं, तो वे अंत में परमाणु रूपांतरण से गुजरते हैं, अर्थात वे एक नया रासायनिक तत्व बन जाते हैं। इस प्रकार, अत्यधिक भारी तत्वों, जैसे कि एनएच, को प्रयोगशाला में उत्पादित किया जाना चाहिए, जो इसे बनाता है a सिंथेटिक रासायनिक तत्व.
एनएच, अन्य अतिभारी तत्वों की तरह, से प्रभावित होता है सापेक्ष प्रभाव - एक सरल तरीके से, सापेक्षता के कारण, जो देखा जाता है, उससे दूरियों की अपेक्षा की जाती है। इस प्रकार, सैद्धांतिक क्षेत्र में गणितीय अध्ययन, जो सापेक्षतावादी प्रभाव के परिणामों का अनुकरण करते हैं, ने बताया कि निहोनियम क्वार्ट्ज के साथ कमजोर रूप से बातचीत कर सकता है, लेकिन रखने के लिए अच्छा सोखना सोना, अपने हल्के समकक्ष, थैलियम (Tl) की तरह।
प्रारंभिक सैद्धांतिक अध्ययनों ने यह भी संकेत दिया अस्थिरता एनएच से क्वार्ट्ज के सोखने के लिए, थैलियम आसानी से TlOH बनाता है, उदाहरण के लिए, और निहोनियम को ऐसा करने का संदेह है।
फिर भी कैसे अध्ययन अभी भी बहुत प्रारंभिक और हाल के हैं, जो कुछ उत्पादित किया गया है वह चर्चा के लिए खुला है, और निहोनियम के भौतिक-रासायनिक गुणों को सटीक रूप से निर्धारित करना मुश्किल है।
निहोनियम प्राप्त करना
तत्व 113, आज तक, दो तरीकों से प्राप्त किया गया है: के माध्यम से शीत संलयन प्रतिक्रियाएं, जस्ता (Zn, Z = 30) के साथ बिस्मथ (Bi, Z = 83) के संलयन के साथ, और इसके माध्यम से भी तत्व 115. का अल्फा क्षय.
पहले उदाहरण में, जस्ता 10% के लिए त्वरित है प्रकाश कि गति, दो नाभिकों की प्रतिकारक शक्तियों को दूर करने के लिए। तब एक आइसोटोप का उत्पादन किया जाता है 279एनएच, जो अंत में एक न्यूट्रॉन का उत्सर्जन करता है और का उत्पादन करता है 278एनएच

लगभग 34 मिलीसेकंड के आधे जीवन के साथ, समस्थानिक 278एनएच तत्व मेंडेलीवियम (एमडी) के लिए छह अल्फा क्षय (अल्फा कण उत्सर्जन) से गुजरता है।
दूसरे मामले में, तत्व 113 संश्लेषित होने के बाद तत्व 115 (अब मस्कोवियम के रूप में जाना जाता है) के अल्फा क्षय से उत्पन्न होता है। एक तरीका आयनों की गर्म संलयन प्रतिक्रिया है 48आइसोटोप के साथ सीए 243आह, उत्पादन 288Mc और फिर, अल्फा क्षय द्वारा, the 284एनएच, जो अल्फा क्षय से गुजरना जारी रखता है।
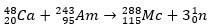
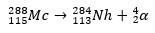
यह भी देखें: हैसियम - अपने गुणों का विश्लेषण करने के लिए सबसे भारी सिंथेटिक रासायनिक तत्व
निहोनियम का इतिहास
तत्व 113 की खोज 2003 में शुरू हुई थी। रिकेन इंस्टीट्यूट के जापानी शोधकर्ताओं ने. के समस्थानिकों को त्वरित किया 70Zn प्रकाश की गति के 10% से टकराने के लिए 209द्वि, एक संलयन प्रतिक्रिया के माध्यम से। इस प्रकार, वे वह उत्पादन करने में कामयाब रहे जिसे हम अब जानते हैं 278एनएच
हालाँकि, यह केवल 2012 में था जापानी शोधकर्ता पूर्ण अल्फा क्षय श्रृंखला का पता लगाने में सक्षम थे तत्व 113 का, खोज का दावा करने के लिए IUPAC से संपर्क करना।
जापानी प्रयासों के साथ, रूसी वैज्ञानिकों ने यूरी ओगेनेशियन के नेतृत्व में, के सहयोग से अमेरिकी वैज्ञानिकों ने भी तत्व के अल्फा क्षय के माध्यम से तत्व 113 की पहचान की 115. इस तरह के प्रयोगों ने रूसी और अमेरिकी वैज्ञानिकों को भी तत्व 113 की मान्यता के लिए विवाद में डाल दिया।

हालांकि, आईयूपीएसी ने रिकेन संस्थान के सबूतों को और अधिक ठोस पाया, और इसलिए जापानियों को तत्व 113 के नाम का अधिकार प्राप्त करने की अनुमति दी। देश के संदर्भ में चुना गया नाम निहोनियो, प्रतीक एनएच था जापान. जापान शब्द जापानी द्वारा दो चीनी अक्षरों का उपयोग करके लिखा गया है जिसका अर्थ है "उगते सूरज की भूमि" और निहोन या निप्पॉन के रूप में पढ़ा जाता है।
निहोनियम नाम इसलिए भी चुना गया क्योंकि 1908 में जापानी रसायनज्ञ मासाताका ओगावा ने प्रकाशित किया था कि तत्व 43 की खोज की थी, इसे जापानी नाम दिया, प्रतीक Np (जो आज नेपच्यूनियम से संबंधित है, Z = 93). हालांकि, बाद में, यह साबित हुआ कि तत्व 43 अस्थिर था, प्रकृति में नहीं पाया जा रहा था और केवल 1937 में संश्लेषित किया गया था, जिसका नाम प्राप्त हुआ था टेक्नेटियम (टीसी)।
इस प्रकार, जापानी आवर्त सारणी से गायब हो गए। हालांकि, वर्षों बाद, यह साबित हो गया कि, वास्तव में, ओगावा ने तत्व 75 (जिसे अब के रूप में जाना जाता है) की खोज की थी रेनीयाम). हालांकि, उस समय तक, रेनियम तत्व को आधिकारिक तौर पर 1925 में खोजा जा चुका था और बपतिस्मा लिया गया था।
निहोनियम पर हल किए गए अभ्यास
प्रश्न 1
निहोनियम, प्रतीक एनएच और परमाणु संख्या 113, एक रासायनिक तत्व है जो अपने छोटे आधे जीवन के कारण प्रकृति में नहीं पाया जा सकता है। उनमें से सबसे स्थायी, 286एनएच, लगभग 9.5 सेकंड है। यह जानते हुए कि आधा जीवन प्रजातियों की मात्रा को आधा करने के लिए आवश्यक समय है, उपरोक्त आइसोटोप की मात्रा राशि का 1/16 होने में कितने सेकंड लगते हैं प्रारंभिक?
ए) 9.5
बी) 19
सी) 28.5
डी) 38
ई) 47.5
संकल्प:
वैकल्पिक डी
प्रत्येक 9.5 सेकंड में, आइसोटोप की मात्रा आधी हो जाती है। तो, 9.5 सेकंड के बाद, इसकी राशि प्रारंभिक राशि का आधा है। एक और 9.5 सेकंड, कुल 19 सेकंड, राशि फिर से आधी हो जाती है, प्रारंभिक के 1/4 तक पहुंच जाती है।
28.5 सेकंड में, एक और आधे जीवन काल के बाद, राशि फिर से आधी हो जाती है, प्रारंभिक राशि के 1/8 तक पहुंच जाती है। अंत में, 38 सेकंड के बाद, राशि फिर से आधी हो जाती है, प्रारंभिक राशि के 1/16 तक पहुंच जाती है, जैसा कि विवरण में अनुरोध किया गया है। इस प्रकार, आवश्यक समय 38 सेकंड है।
प्रश्न 2
2003 में, जापान में रिकेन इंस्टीट्यूट में तत्व 113 की खोज शुरू हुई। उस समय, वैज्ञानिक इसका उत्पादन करने में सक्षम थे 278जस्ता और बिस्मथ परमाणुओं के संलयन के माध्यम से एनएच।
उद्धृत समस्थानिक में कितने न्यूट्रॉन हैं?
ए) 113
बी) 278
सी) 391
डी) 170
ई) 165
संकल्प:
वैकल्पिक ई
की संख्या न्यूट्रॉन के रूप में गणना की जा सकती है:
ए = जेड + एन
जहाँ A की संख्या है पास्ता परमाणुZ परमाणु क्रमांक है और n न्यूट्रॉनों की संख्या है। मूल्यों को प्रतिस्थापित करते हुए, हमारे पास है:
278 = 113 + n
एन = 278 - 113
एन = 165
स्टेफ़ानो अराउजो नोवाइस द्वारा
रसायन विज्ञान शिक्षक