इलेक्ट्रॉनिक वितरण से तात्पर्य है कि परमाणु के नाभिक को घेरने वाली परतों या ऊर्जा स्तरों में इलेक्ट्रॉनों को कैसे वितरित किया जाता है।
रदरफोर्ड-बोहर परमाणु मॉडल के अनुसार, ज्ञात रासायनिक तत्वों के परमाणुओं में अधिकतम सात. होते हैं इलेक्ट्रॉनिक परतें, जो कोर के अंदर से बाहर तक ऊर्जा में वृद्धि करती हैं (1 - 2 - 3 - 4 - 5 - 6 - 7). इन सात परतों को संबंधित अक्षर K - L - M - N - O - P - Q द्वारा भी निर्दिष्ट किया जा सकता है, जिसमें K पहला है, नाभिक के करीब है और सबसे कम ऊर्जा वाला है। दूसरी ओर, क्यू परत सातवीं है, जो कोर से सबसे दूर है और उच्चतम ऊर्जा वाला है।
चूंकि प्रत्येक परमाणु की एक परमाणु संख्या (नाभिक में प्रोटॉन की मात्रा) और इलेक्ट्रॉनों की एक अलग संख्या होती है, इसलिए प्रत्येक परमाणु की इलेक्ट्रॉन परतों में अलग-अलग ऊर्जाएँ होती हैं जो उस ऊर्जा के साथ इलेक्ट्रॉनों को धारण करती हैं निर्धारित।
माइंड मैप: इलेक्ट्रॉनिक डिस्ट्रीब्यूशन

* माइंड मैप को पीडीएफ में डाउनलोड करने के लिए, यहां क्लिक करें!
उनके इलेक्ट्रॉनिक परतों में वितरित कुछ परमाणुओं और इलेक्ट्रॉनों के नीचे नोट करें:

हाइड्रोजन, हीलियम, बेरिलियम और ऑक्सीजन परमाणु
ध्यान दें कि बेरिलियम के चार परमाणुओं का वितरण है: 2 - 2, और ऑक्सीजन का वितरण 2 - 6 है। केवल इन उदाहरणों के माध्यम से यह देखना संभव है कि इलेक्ट्रॉनिक वितरण एक आदेश का पालन करता है। उदाहरण के लिए, K (1) शेल में अधिकतम दो इलेक्ट्रॉन हो सकते हैं।
नीचे हमारे पास एक सारणी है जो प्रत्येक इलेक्ट्रॉनिक परत में वितरित किए जा सकने वाले इलेक्ट्रॉनों की अधिकतम मात्रा को निर्दिष्ट करती है:
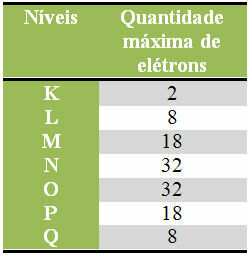
इलेक्ट्रॉनिक स्तरों में इलेक्ट्रॉनों की अधिकतम संख्या
यह भी याद रखना चाहिए कि भरा जाने वाला अंतिम कोश, तथाकथित संयोजकता कोश, में अधिकतम आठ इलेक्ट्रॉन होने चाहिए। इसलिए यदि आपने इलेक्ट्रॉनों को वितरित किया और देखा कि अंतिम शेल की मात्रा 8 से अधिक थी, लेकिन छोटी थी उस 18 को, उस शेल में केवल 8 इलेक्ट्रॉनों को छोड़ना चाहिए और बाकी को अगले शेल में जोड़ना चाहिए बाहरी।
अब मत रोको... विज्ञापन के बाद और भी बहुत कुछ है;)
उदाहरण के लिए, कैल्शियम परमाणु के इलेक्ट्रॉनिक वितरण पर विचार करें। आवर्त सारणी को देखते हुए, हम देखते हैं कि इसकी परमाणु संख्या 20 के बराबर है, जबकि जमीनी अवस्था में इलेक्ट्रॉनों की संख्या समान होती है। इसलिए, हमें 20 इलेक्ट्रॉनों को उनके इलेक्ट्रॉन कोशों में वितरित करना होगा। इसे नीचे देखें:
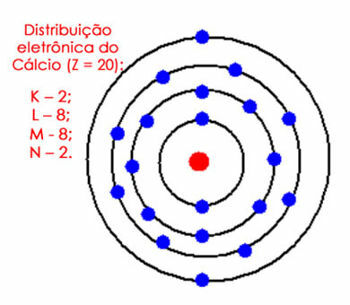
परमाणु में कैल्शियम का इलेक्ट्रॉनिक वितरण
ध्यान दें कि M शेल 18 इलेक्ट्रॉनों को धारण कर सकता है, लेकिन यदि हम इसमें शेष इलेक्ट्रॉनों को रखते हैं, तो इसमें 10 इलेक्ट्रॉन होंगे, जो कि वैलेंस शेल में नहीं हो सकता है। इसलिए हम अन्य इलेक्ट्रॉनों (2) को अगले कोश में रखते हैं, जो कि N है।
लेकिन यदि अंतिम कोश में इलेक्ट्रॉनों की मात्रा 18 और 32 के बीच है, तो आप 18 इलेक्ट्रॉनों को छोड़ देते हैं और शेष को बाहरी कोश में भेज देते हैं। एक और उदाहरण देखें:
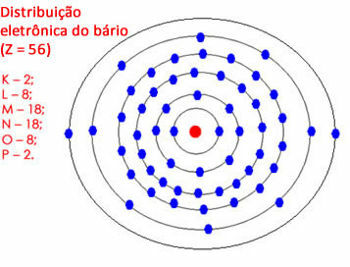
परमाणु में बेरियम का इलेक्ट्रॉनिक वितरण
ध्यान दें कि "एन" शेल में अधिकतम 32 इलेक्ट्रॉन हो सकते हैं, लेकिन यहां यह 28 होगा। तो हम 18 इलेक्ट्रॉनों को छोड़ देते हैं और बाकी को अगले कोश में भेज देते हैं। लेकिन "O" शेल में 10 इलेक्ट्रॉन होंगे, इसलिए हमने 8 को छोड़ दिया और शेष 2 इलेक्ट्रॉनों को "P" शेल में वितरित कर दिया।
हालांकि, परमाणु के इलेक्ट्रॉनों के इस इलेक्ट्रॉनिक वितरण को करने का एक आसान तरीका है। यह के माध्यम से है पॉलिंग आरेख (चूंकि यह वैज्ञानिक लिनुस कार्ल पॉलिंग (1901-1994) द्वारा बनाया गया था), जिसे के रूप में भी जाना जाता है इलेक्ट्रॉनिक वितरण आरेख या फिर भी, ऊर्जा स्तरों का आरेख. यह आरेख इस तरह दिखता है:
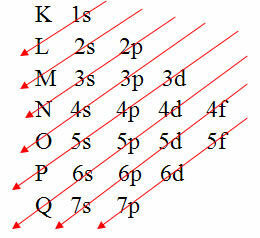
इलेक्ट्रॉनिक वितरण का चित्रमय प्रतिनिधित्व पॉलिंग आरेख द्वारा दिया गया है
यह समझने के लिए कि इस आरेख में इलेक्ट्रॉनों और आयनों का इलेक्ट्रॉनिक वितरण कैसे किया जाता है, नीचे दिए गए पाठ पढ़ें:
* इलेक्ट्रॉन वितरण;
* इलेक्ट्रॉनिक आयन वितरण.
* लिनुस पॉलिंग से छवि क्रेडिट: नोबेलप्राइज.ओआरजी
** मेरे द्वारा माइंड मैप। डिओगो लोपेज
जेनिफर फोगाका द्वारा
रसायन विज्ञान में स्नातक
क्या आप इस पाठ को किसी स्कूल या शैक्षणिक कार्य में संदर्भित करना चाहेंगे? नज़र:
FOGAÇA, जेनिफर रोचा वर्गास। "इलेक्ट्रॉनिक वितरण क्या है?"; ब्राजील स्कूल. में उपलब्ध: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-distribuicao-eletronica.htm. 27 जुलाई, 2021 को एक्सेस किया गया।
रसायन शास्त्र

नील्स बोहर, बोहर का परमाणु, परमाणु भौतिकी, स्थिर परमाणु, परमाणु मॉडल, ग्रह प्रणाली, इलेक्ट्रोस्फीयर की परतें, ऊर्जा स्तर, इलेक्ट्रॉन गोले, इलेक्ट्रॉन ऊर्जा, रदरफोर्ड परमाणु मॉडल, उत्तेजित अवस्था परमाणु।


