अम्ल वर्षा ऑक्साइड द्वारा निर्मित होती है: सल्फर डाइऑक्साइड (SO .)2) और नाइट्रोजन (NO .)2), दोनों जलते कोयले, जीवाश्म ईंधन और औद्योगिक प्रदूषकों से प्राप्त हुए हैं।
केवल2 और नहीं2 वे तब हमारे वायुमंडल के घटक बन जाते हैं। और इसलिए समस्या पैदा होती है: ये गैसें, वातावरण में मौजूद हाइड्रोजन (जलवाष्प) के साथ मिलकर सल्फ्यूरिक एसिड और नाइट्रिक एसिड से भरी बारिश को जन्म देती हैं। जैसा कि देखा जा सकता है, इन अम्लों की उपस्थिति ही वर्षा को अम्लीय बनाती है।
जब अम्लीय वर्षा सतह पर गिरती है, तो यह एक महान पर्यावरणीय प्रभाव का कारण बनती है, मिट्टी और पानी की रासायनिक संरचना को बदल देती है, खाद्य श्रृंखलाओं को प्रभावित करती है, और जंगलों और फसलों को नष्ट कर देती है। क्या अधिक है, वे न केवल ग्रामीण इलाकों में, बल्कि शहरों में भी नुकसान पहुंचाते हैं: वे धातु संरचनाओं, ऐतिहासिक स्मारकों (मूर्तियों) और इमारतों को खराब करते हैं।
आइए इन अम्लों की क्रिया के बारे में थोड़ा और जानें:
→ सल्फ्यूरिक अम्ल (एच2केवल4)
यह एसिड अपनी ऊर्जावान क्रिया (निर्जलीकरण) के कारण कागज, सूती कपड़े, लकड़ी, चीनी और अन्य सामग्री को नष्ट कर सकता है। कल्पना कीजिए कि बारिश में मौजूद होने पर इससे क्या नुकसान होता है?
जीवित जीवों के ऊतकों पर सल्फ्यूरिक एसिड का संक्षारक प्रभाव होता है। सल्फर डाइऑक्साइड से प्रदूषित वातावरण में बनने वाली वर्षा में H. होता है2केवल4, जो एक महान विनाशकारी प्रभाव का कारण बनता है, उदाहरण के लिए संगमरमर जैसे संक्षारक पौधों, धातुओं और यहां तक कि पत्थरों की अपनी संपत्ति के कारण।
→ नाइट्रिक अम्ल (HNO3)
नाइट्रोजन ऑक्साइड (NO) से प्रदूषित वातावरण में उत्पन्न होने वाली अम्लीय वर्षा में इसकी संरचना में अम्ल HNO होता है3.
नाइट्रिक एसिड जहरीला होता है और सल्फ्यूरिक एसिड की तरह यह संक्षारक होता है और प्रकृति को बहुत नुकसान पहुंचाता है।
माइंड मैप: एसिड रेन
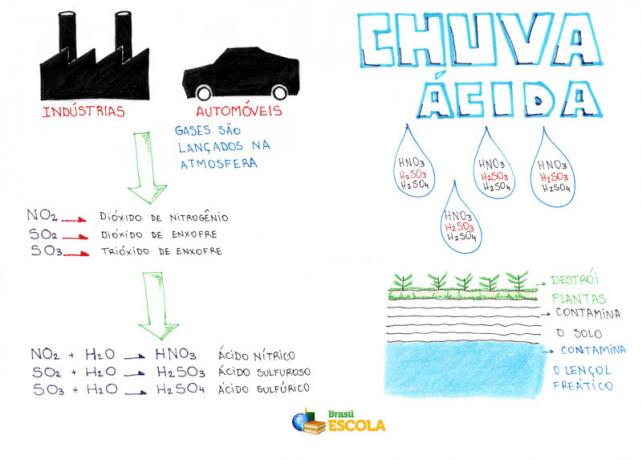
*मानसिक मानचित्र को PDF में डाउनलोड करने के लिए, यहाँ क्लिक करें!
लिरिया अल्वेस द्वारा
रसायन विज्ञान में स्नातक
स्रोत: ब्राजील स्कूल - https://brasilescola.uol.com.br/quimica/quimica-chuva-acida.htm
