पर जलयोजन प्रतिक्रियाएं अल्काडीनेस वो हैं जोड़ प्रतिक्रियाएंयानी पानी के अणु के घटकों (हाइड्रोनियम और हाइड्रॉक्साइड) को एक एल्केडियन में जोड़ा जाता है।
आप अल्काडीनेस वे हाइड्रोकार्बन हैं जिनकी कार्बन के बीच एक खुली श्रृंखला और दो दोहरे बंधन (एक सिग्मा और एक पाई द्वारा निर्मित) होते हैं, जैसा कि हम निम्नलिखित संरचना में देख सकते हैं:

एल्काडीन का संरचनात्मक सूत्र
के लिए एल्केडीनेस में जलयोजन प्रतिक्रिया किया जाता है, तो यह आवश्यक है कि द्विबंध में उपस्थित पाई आबंध ऊष्मा तथा सल्फ्यूरिक अम्ल (H) के प्रभाव से टूट जाए।2केवल4). पाई बॉन्ड के टूटने के साथ, दो बॉन्ड साइट दिखाई देती हैं, प्रत्येक डबल बॉन्ड में शामिल कार्बन में से एक पर।

पीआई बंधन के विघटन के साथ बाध्यकारी साइटों का उदय
आयनों (H) के लिए एल्काडीन अणु पर बाध्यकारी साइटों की उपस्थिति आवश्यक है+ और ओह-) पानी से एल्केडीन में मिलाया जाता है, उदाहरण के लिए, एक डायलकोहल (शराब दो हाइड्रॉक्सिल के साथ)।
H. का जोड़+ और ओह- एल्काडीन की संरचना में
ध्यान दें: H का जोड़+ और ओह- एल्केडियन संरचना में निम्नानुसार है मार्कोवनिकोव का नियम, यानी H+ सबसे हाइड्रोजनीकृत कार्बन से बांधता है, और OH- कम हाइड्रोजनीकृत कार्बन से बांधता है।

एल्काडिएन्स के जलयोजन में मार्कोवनिकोव नियम के अनुप्रयोग का उदाहरण
चूंकि दोहरे बंधनों की स्थिति के संबंध में विभिन्न प्रकार के एल्केडीन होते हैं, ऐसा हो सकता है कि एल्काडियन का जलयोजन विभिन्न यौगिकों का निर्माण करता है। निम्नलिखित मामले देखें:
→ संचित या संघनित एल्काडीन
यह एक एल्केडीन है जिसमें एक साथ दो दोहरे बंधन होते हैं जिसमें तीन परमाणु शामिल होते हैं कार्बन, अर्थात्, बंधों में शामिल कार्बन को अलग करने वाला कोई एकल बंधन नहीं है दुगना।

संचित क्षार का संरचनात्मक सूत्र
एक वैकल्पिक एल्काडीन की जलयोजन प्रतिक्रिया के दौरान, पीआई बांड टूट जाते हैं, एच. होने के नाते+ अधिक हाइड्रोजनीकृत कार्बन और OH. में जोड़ा जाता है- कम हाइड्रोजनीकृत कार्बन में जोड़ा गया:
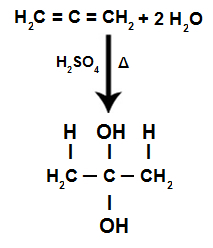
संचित अल्काडीन हाइड्रेशन रिएक्शन समीकरण
हमारे पास यह है कि एक संचित एल्केडियन के जलयोजन में, एक ही कार्बन परमाणु दो हाइड्रॉक्सिल प्राप्त करता है, जिससे एक जुड़वां अल्कोहल बनता है, जो एक अस्थिर संरचना है।

जुड़वां गठित अल्कोहल की संरचना
चूंकि जुड़वां अल्कोहल अस्थिर है, इसलिए हमारे पास दो हाइड्रॉक्सिल के घटकों के साथ एक पानी के अणु का निर्माण होता है और कार्बन और ऑक्सीजन के बीच एक पाई बंधन का निर्माण होता है।

जुड़वां अल्कोहल से कीटोन का निर्माण
इसलिए, संचित एल्केडीन की जलयोजन प्रतिक्रिया के परिणामस्वरूप a. का निर्माण होगा कीटोन.
→ संयुग्मित या वैकल्पिक एल्काडीन
यह एक एल्केडियन है जिसमें एक साथ दो दोहरे बंधन होते हैं जिसमें चार शामिल होते हैं कार्बन परमाणु, अर्थात्, बंधों में शामिल कार्बन को अलग करने वाला एक एकल बंधन होता है दुगना।
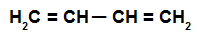
एक वैकल्पिक अल्काडियन का संरचनात्मक सूत्र
अल्काडिएन्स में बारी-बारी से उनके दोहरे बंधनों की प्रतिध्वनि होती है। इस प्रकार, पाई बांड के इलेक्ट्रॉन स्थिति (लाल तीर) बदलते हैं, जैसा कि निम्नलिखित आरेख में है:
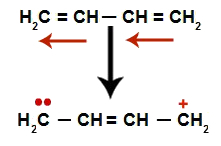
एक वैकल्पिक एल्काडीन में प्रतिध्वनि का चित्रण करने वाला योजनाबद्ध
हमारे पास, सामान्य तौर पर, कार्बन के बीच एक डबल बॉन्ड की उपस्थिति होती है, जहां दो डबल्स पहले थे और दो बंधन स्थलों का निर्माण, प्रत्येक कार्बन पर एक जो अब दोहरा बंधन नहीं बना रहा है (उदाहरण के लिए, कार्बन 1 और 4). श्रृंखला के कार्बन 1 और 4 H. प्राप्त करते हैं+ और ओह- पानी से।

अल्काडीन को बारी-बारी से आंशिक जलयोजन
अनुनाद के बाद, नए दोहरे बंधन का पाई बंधन टूट जाता है, और एक H+ और एक ओह- एल्काडीन अणु में जोड़ा जाता है। OH को पहले जोड़े गए OH समूह के निकटतम कार्बन में जोड़ा जाता है क्योंकि यह समूह के इलेक्ट्रॉनिक आकर्षण से गुजरता है, जो कि अधिक विद्युतीय है।

एक वैकल्पिक एल्काडीन में जलयोजन की समाप्ति
प्रतिध्वनि के कारण, हम कहते हैं कि वैकल्पिक एल्केडीन 1.4 जलयोजन से गुजरता है, जिससे एक डायलकोहल बनता है।
→ अल्काडाइन इंसुलेटेड
यह एक एल्केडियन है जिसमें दो दोहरे बंधन होते हैं जिनमें कम से कम पांच परमाणु एक साथ होते हैं। कार्बन का, अर्थात्, बांड में शामिल कार्बन को अलग करने वाले कम से कम दो एकल बंधन हैं bonds दुगना।

एक पृथक एल्केडियन का संरचनात्मक सूत्र formula
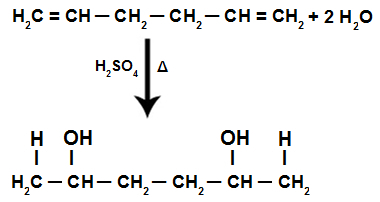
एक पृथक एल्केडियन की जलयोजन प्रतिक्रिया के दौरान, पीआई बांड टूट जाते हैं, एच+ अधिक हाइड्रोजनीकृत कार्बन और OH. में जोड़ा जाता है- कम हाइड्रोजनीकृत कार्बन में जोड़ा गया।

पृथक एल्केडीन जलयोजन प्रतिक्रिया समीकरण
इसलिए, एक पृथक एल्केडियन के अलावा, हमारे पास केवल एक डायल अल्कोहल का गठन होता है।
मेरे द्वारा। डिओगो लोपेज डायस
स्रोत: ब्राजील स्कूल - https://brasilescola.uol.com.br/quimica/reacoes-hidratacao-alcadienos.htm
