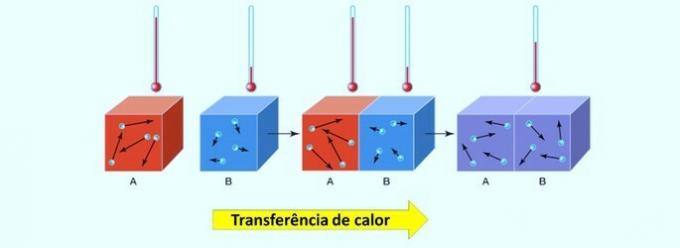
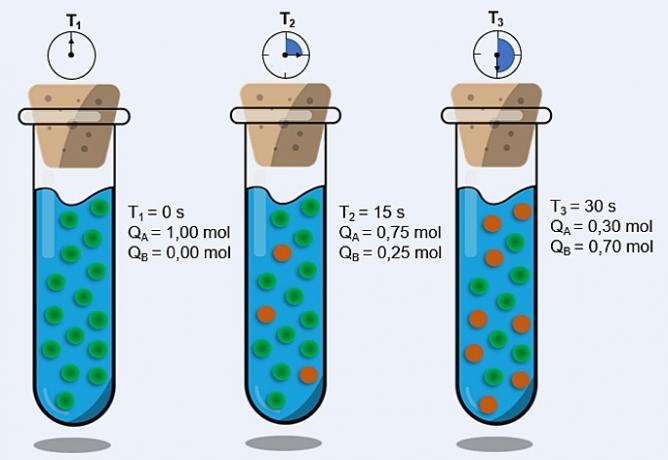
एंडोथर्मिक और एक्ज़ोथिर्मिक प्रतिक्रियाएं हैं मात्राएं जो रासायनिक प्रतिक्रियाओं के दौरान अवशोषित और जारी गर्मी (ऊर्जा) की मात्रा को मापती हैं. इनका अध्ययन थर्मोकैमिस्ट्री द्वारा किया जाता है।
उनमें क्या अंतर है?
ऊष्माशोषी अभिक्रिया वह है जिसमें ऊर्जा अवशोषण होता है। इस प्रक्रिया में, ऊर्जा का उत्पादन और स्वतंत्र रूप से बनाए रखा जाता है।
पक्षियों और स्तनधारियों में स्थिर शरीर के तापमान को बनाए रखने की क्षमता होती है। इस कारण से उन्हें एंडोथर्मिक जानवर कहा जाता है, लोकप्रिय रूप से "गर्म खून वाले जानवर"।
उष्माक्षेपी प्रतिक्रिया वह है जिसमें ऊर्जा रिलीज होती है। इस प्रक्रिया में ऊर्जा उत्पादन केवल ऊर्जा की निरंतर आपूर्ति के माध्यम से ही बना रहता है।
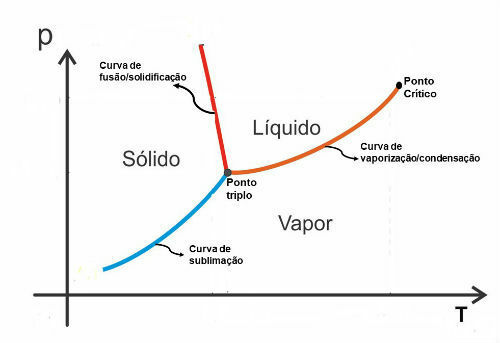
भौतिक अवस्थाओं को उस क्रम में बदलना: गैस, तरल और ठोस, एक एक्ज़ोथिर्मिक प्रतिक्रिया का एक उदाहरण है। उनमें से प्रत्येक तब होता है जब ऊर्जा मुक्त होती है, अर्थात जब कम गर्मी होती है।
ध्यान दें कि जब हम इस क्रम (ठोस, तरल और गैस) को उलटते हैं, तो ऊर्जा उत्पन्न होती है (अधिक गर्मी)। इस मामले में, प्रतिक्रिया एंडोथर्मिक है।
दैनिक उदाहरण
शरीर की चर्बी हमारे शरीर में ईंधन का काम करती है। जो जलता नहीं है, वह उसमें समा जाता है। चूंकि यह एक अवशोषण प्रक्रिया है, यह एक एंडोथर्मिक प्रतिक्रिया का एक उदाहरण है।
भोजन तैयार करने के लिए पैन को आग पर रखते समय, हम बदले में एक ऊष्माक्षेपी प्रक्रिया का सामना कर रहे होते हैं। ऐसा इसलिए है क्योंकि जो गर्मी निकलती है वह इस भोजन को बदल देगी ताकि इसका सेवन किया जा सके।
और एन्थैल्पी क्या है?
तापीय धारिता यह वह ऊर्जा है जो सभी पदार्थों में मौजूद है और जो एंडोथर्मिक और एक्ज़ोथिर्मिक प्रतिक्रियाओं के परिणामस्वरूप बदल जाती है।
चूंकि एन्थैल्पी की गणना करना संभव नहीं है, इसलिए इसकी भिन्नता की गणना स्थापित की गई थी।
इस प्रकार, मानक एन्थैल्पी (1atm के वायुमंडलीय दबाव के तहत 25ºC का तापमान) की तुलना करके, एन्थैल्पी भिन्नता की गणना करना संभव होगा।
के अनुसार हेस का कानून, अंतिम एन्थैल्पी घटा प्रारंभिक एन्थैल्पी (एच = एचएफ - होमैं) इस डेटा में परिणाम।
यदि एंडोथर्मिक प्रतिक्रिया ऊर्जा को अवशोषित करती है, तो इसका मतलब है कि (अंतिम) अभिकारक की थैलीपी (प्रारंभिक) उत्पाद की तुलना में कम है। अत: एन्थैल्पी परिवर्तन धनात्मक है (ΔH > 0)।
बदले में, यदि एक्ज़ोथिर्मिक प्रतिक्रिया ऊर्जा जारी करती है, तो इसका मतलब है कि अभिकारक की ऊर्जा (ऊर्जा) उत्पाद की तुलना में अधिक है। इसलिए, एन्थैल्पी भिन्नता ऋणात्मक है (ΔH
यह भी पढ़ें:
- रसायनिक प्रतिक्रिया
- रासायनिक संतुलन
- दहन