संवयविता यह एक प्राकृतिक घटना है जिसमें विभिन्न पदार्थों (रासायनिक और भौतिक गुणों के संदर्भ में) के समान आणविक सूत्र होते हैं, जैसा कि निम्नलिखित उदाहरण में है:
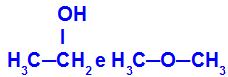
विभिन्न पदार्थ जिनका आणविक सूत्र समान होता है
इथेनॉल (बाएं) का आणविक सूत्र C. है2एच6O, जो मेथॉक्सीथेन (दाएं) के साथ भी होता है, इसलिए वे समावयवी हैं।
आइसोमेरिज्म के प्रकार
→ समतल समावयवी
यह आइसोमेरिज्म का प्रकार है जो आइसोमर्स के बीच संरचनात्मक अंतर का अध्ययन करता है।
द) व्यवसाय
यह समतल समरूपता का प्रकार है जिसमें पदार्थों के बीच का अंतर उन कार्बनिक कार्यों के बीच के अंतर पर आधारित होता है जिनसे वे संबंधित हैं। कुछ उदाहरण देखें:
प्रोपेनोन और प्रोपेन:
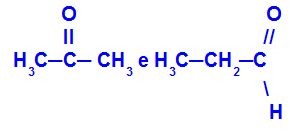
विभिन्न कार्यों से संबंधित आइसोमर्स
प्रोपेनोन (बाएं) कीटोन समूह से संबंधित है, और प्रोपेनल (दाएं) एल्डिहाइड समूह से संबंधित है।
बी) जेल
यह समतल समरूपता का प्रकार है जिसमें पदार्थों के बीच का अंतर उनके द्वारा मौजूद जंजीरों के बीच के अंतर पर आधारित होता है। एक उदाहरण देखें:
2-मिथाइल-प्रोपेन और ब्यूटेन
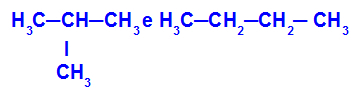
आइसोमर्स जिनमें विभिन्न वर्गीकरणों के साथ श्रृंखलाएं होती हैं
उदाहरण में, हम देख सकते हैं कि 2-मिथाइल-प्रोपेन (बाईं ओर) में एक शाखित श्रृंखला होती है, और ब्यूटेन (दाईं ओर) में एक सामान्य श्रृंखला होती है।
सी) पद
यह समतल समावयवता का प्रकार है जिसमें पदार्थों के बीच का अंतर उनकी जंजीरों में मौजूद एक घटक की स्थिति के अंतर पर आधारित होता है। एक उदाहरण देखें:
1-क्लोरो-प्रोपेन और 2-क्लोरो-प्रोपेन
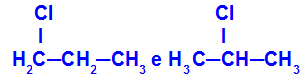
श्रृंखला में विभिन्न पदों पर घटक रखने वाले आइसोमर्स
उदाहरण में, हम देख सकते हैं कि 1-क्लोरो-प्रोपेन (बाईं ओर) में कार्बन 1 पर क्लोरीन स्थित है, और 2-क्लोरो-प्रोपेन (दाईं ओर) में क्लोरीन कार्बन 2 पर स्थित है।
घ) मेटामेरिया या मुआवजा
ध्यान दें: समरूपता विशेष रूप से विषम तारों के लिए मान्य है।
यह फ्लैट आइसोमेरिज्म का प्रकार है जिसमें पदार्थों के बीच का अंतर उनकी जंजीरों में मौजूद हेटेरोएटम की स्थिति में अंतर पर आधारित होता है। एक उदाहरण देखें:
उदाहरण: मेथॉक्सीप्रोपेन और एथोक्सीथेन
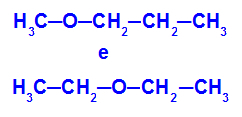
श्रृंखला में विभिन्न पदों पर विषम परमाणु वाले आइसोमर्स
उदाहरण में, हम देख सकते हैं कि, मेथॉक्सीप्रोपेन (बाएं) में, ऑक्सीजन में एक तरफ एक कार्बन और दूसरी तरफ तीन कार्बन के साथ एक रेडिकल होता है। एथोक्सीथेन (दाएं) में, ऑक्सीजन में एक तरफ दो कार्बन और दूसरी तरफ दो कार्बन होते हैं।
तथा)टॉटोमेरी
यह समतल फलन समरूपता का एक विशेष मामला है और केवल तीन कार्बनिक कार्यों में होता है:
एल्डिहाइड
कीटोन
एनोलो
इस प्रकार का समावयवता इस तथ्य पर कार्य करता है कि एक एनोल और एक एल्डिहाइड के बीच एक रासायनिक संतुलन होता है और एक एनोल और एक कीटोन के बीच, अर्थात ये घटक लगातार एक दूसरे में परिवर्तित हो रहे हैं। एक उदाहरण देखें:
प्रोप-2-एन-1-ओएल और प्रोपेनोन
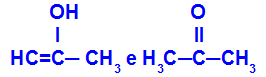
विभिन्न कार्यों से संबंधित आइसोमर्स
उदाहरण में, हम देख सकते हैं कि Prop-2-en-1-ol (बाईं ओर) एनोल के समूह से संबंधित है, और प्रोपेनोन (दाईं ओर) केटोन्स के समूह से संबंधित है, इसलिए वे टॉटोमेरी के आइसोमर्स हैं।
→ अंतरिक्ष समरूपता
यह अणु के स्थानिक विश्लेषण द्वारा परिभाषित एक प्रकार का समरूपता है।
ए) ज्यामितीय आइसोमर
अब मत रोको... विज्ञापन के बाद और भी बहुत कुछ है;)
यह एक प्रकार का स्थानिक समरूपता है जो तब होता है जब पदार्थ में निम्नलिखित विशेषताओं वाले अणु होते हैं:
बंद श्रृंखला जिसमें दो अलग-अलग लिगेंड के साथ दो कार्बन होते हैं, जैसा कि नीचे दिए गए उदाहरण में है:

ज्यामितीय समरूपता के साथ बंद संरचना
खुली श्रृंखला जिसमें कार्बन के बीच एक दोहरा बंधन होता है और, दोहरे बंधन के इनमें से प्रत्येक कार्बन में, दो अलग-अलग लिगैंड होते हैं, जैसा कि नीचे दिए गए उदाहरण में है:
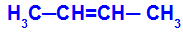
ज्यामितीय समरूपता के साथ खुली संरचना
ज्यामितीय समरूपता दो समूहों में विभाजित है:
1हे समूह: सिस-ट्रांस
यह तब होता है जब एक कार्बन के दो लिगैंड दूसरे कार्बन के दो लिगैंड के बराबर होते हैं, चाहे वह खुली संरचना में हो या बंद संरचना में।
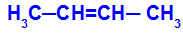
एक पदार्थ की श्रृंखला जिसमें सीआईएस-ट्रांस आइसोमेरिज्म होता है
आइसोमर को सीआईएस कहा जाएगा जब एक ही लिगैंड एक ही विमान में हों।

सीआईएस आइसोमर का उदाहरण
आइसोमर को ट्रांस कहा जाएगा जब विभिन्न लिगैंड एक ही विमान में हों।

ट्रांस आइसोमर का उदाहरण
2हे समूह: ई-जेड
यह तब होता है जब एक कार्बन के दो लिगैंड दूसरे कार्बन के दो लिगैंड के संबंध में भिन्न होते हैं, या तो खुली संरचना में या बंद संरचना में।

एक पदार्थ की श्रृंखला जिसमें E-Z समावयवता है
आइसोमर को ई कहा जाएगा जब उच्चतम परमाणु संख्या वाले लिगैंड विपरीत विमानों में हों। नीचे दिए गए उदाहरण में, बाईं ओर कार्बन में सबसे अधिक परमाणु संख्या (35) के साथ Br है और दूसरे में ऑक्सीजन (8) है।
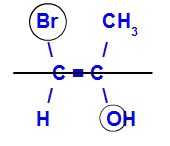
ई-आइसोमर का उदाहरण
आइसोमर को Z कहा जाएगा जब उच्चतम परमाणु संख्या वाले लिगैंड एक ही विमान में हों। नीचे दिए गए उदाहरण में, बाईं ओर कार्बन में सबसे अधिक परमाणु संख्या (35) के साथ Br है और दूसरे में ऑक्सीजन (8) है।

Z-आइसोमर का उदाहरण
बी) ऑप्टिकल आइसोमर
यह एक प्रकार का स्थानिक समरूपता है जो केवल तभी होता है जब पदार्थ में अणु होते हैं चिरल कार्बन (वह जिसमें चार अलग-अलग लिगेंड हैं) उनकी संरचनाओं में। चिरल कार्बन वाले अणु में प्रकाश को ध्रुवीकृत और विक्षेपित करने की क्षमता होती है, जो इस प्रकार है:
दाईं ओर (दाएं हाथ का आइसोमर)
बाईं ओर (लेवरोटेटरी आइसोमर)
प्रकाशिक गतिविधि वाले यौगिक में हमेशा होता है सक्रिय आइसोमर्स (ऑप्टिकल एंटीपोड कहा जाता है) और निष्क्रिय आइसोमर्स (दो सक्रिय आइसोमर्स के बीच का मिश्रण, एक मिश्रण जिसे रेसमिक कहा जाता है)।
चिरल कार्बन वाले यौगिक के सक्रिय (IOA) और निष्क्रिय (IOI) आइसोमर्स की संख्या निर्धारित करने के लिए हम निम्नलिखित सूत्र का उपयोग कर सकते हैं:
आईओए = 2नहीं न
आईओआई = 2नहीं न
2
नीचे एक यौगिक का उदाहरण दिया गया है जिसमें ज्यामितीय समरूपता है:
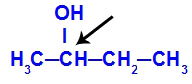
ब्यूटेन-2-ओल. में चित्रित चिरल कार्बन
Butan-2-ol की संरचना में निम्नलिखित लिगेंड हैं:
मिथाइल (सीएच3)
एथिल (सीएच3-सीएच2)
हाइड्रोजन (एच)
हाइड्रॉक्सिल (OH)
क्योंकि इसमें केवल एक चिरल कार्बन होता है, इसलिए ब्यूटेन-2-ओल में होता है:
सक्रिय आइसोमर्स:
आईओए = 21
आईओए = 2
निष्क्रिय आइसोमर्स:
आईओआई = 21
2
आईओआई = 2
2
आईओआई = 1
मेरे द्वारा। डिओगो लोपेज डायस
क्या आप इस पाठ को किसी स्कूल या शैक्षणिक कार्य में संदर्भित करना चाहेंगे? देखो:
DAYS, डिओगो लोपेज। "समरूपता क्या है?"; ब्राजील स्कूल. में उपलब्ध: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-isomeria.htm. 27 जून, 2021 को एक्सेस किया गया।