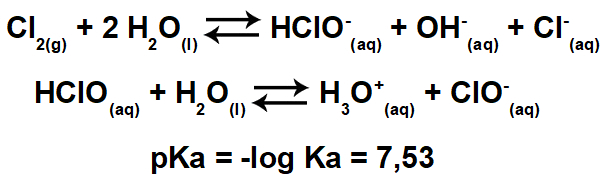कई दवाओं में और तरल और ठोस खाद्य उत्पादों में, जैसे सिरका और बिस्कुट, उदाहरण के लिए, विलेय के प्रतिशत द्रव्यमान में सामग्री (m1) पूरे समाधान के द्रव्यमान के संबंध में (एम = एम1 + एम2). इस परिमाण को कहा जाता है शीर्षक (टी) या द्रव्यमान प्रतिशत एक समाधान का।
इसकी परिभाषा इस प्रकार व्यक्त की जा सकती है:

इस प्रकार, इसकी गणना नीचे दिए गए गणितीय समीकरण के माध्यम से की जाती है:
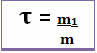
या

चूंकि हर और अंश दोनों एक ही इकाई (द्रव्यमान इकाई ग्राम - जी) के साथ काम कर रहे हैं, शीर्षक की कोई इकाई नहीं है और 1 से कम है।
इस प्रकार, यदि हम कहते हैं कि किसी दिए गए समाधान का शीर्षक 0.4 है, तो इसका मतलब है कि समाधान के द्रव्यमान की प्रत्येक इकाई के लिए, 0.4, विलेय के द्रव्यमान से मेल खाती है। हालाँकि, शीर्षक को अक्सर प्रतिशत के रूप में व्यक्त किया जाता है। ऐसा करने के लिए, बस पाए गए मान को 100% से गुणा करें। इस मामले में इसे कहा जाता है मास प्रतिशत (टी%) *
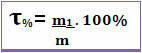
नीचे दिए गए चित्र पर ध्यान दें, जिसमें लवणीय विलयन में सोडियम क्लोराइड के द्रव्यमान का प्रतिशत दिया गया है

निर्जलीकरण के उपचार में उपयोग किए जाने वाले खारा में 0.9% सोडियम क्लोराइड का द्रव्यमान प्रतिशत होता है
अब मत रोको... विज्ञापन के बाद और भी बहुत कुछ है;)
इस मामले में, इसका मतलब है कि इस घोल की प्रत्येक 100 ग्राम या 100 इकाइयों के लिए, 0.9 ग्राम या 0.9% विलेय, यानी सोडियम क्लोराइड (NaCl - टेबल सॉल्ट) होता है।
एक और उदाहरण सिरका है: इसके लेबल पर एक संकेत है कि इसकी तैयारी में एसिटिक एसिड के द्रव्यमान का 5% उपयोग किया गया था, यानी प्रत्येक 100 ग्राम समाधान के लिए इस एसिड के 5 ग्राम हैं।

शीर्षक में भी दिया जा सकता है मात्रा प्रतिशत. इस मामले में, अंतर केवल इतना है कि विलेय के द्रव्यमान को विलयन के द्रव्यमान से जोड़ने के बजाय; निम्नलिखित सूत्र के अनुसार विलेय का आयतन विलयन के आयतन से संबंधित होता है:
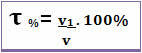
उदाहरण के लिए, नियमित अल्कोहल के मामले में, जिसकी मात्रा ९६% है, १०० एमएल घोल में, ९६ एमएल अल्कोहल है।

* शब्द "शीर्षक" वैज्ञानिकों के बीच अधिक उपयोग किया जाता है, जबकि तकनीशियन और कई पुस्तक लेखक "मास प्रतिशत" अभिव्यक्ति का अधिक बार उपयोग करते हैं।
जेनिफर फोगाका द्वारा
रसायन विज्ञान में स्नातक
क्या आप इस पाठ को किसी स्कूल या शैक्षणिक कार्य में संदर्भित करना चाहेंगे? देखो:
FOGAÇA, जेनिफर रोचा वर्गास। "शीर्षक या द्रव्यमान प्रतिशत"; ब्राजील स्कूल. में उपलब्ध: https://brasilescola.uol.com.br/quimica/titulo-ou-porcentagem-massa.htm. 28 जून, 2021 को एक्सेस किया गया।