की अवधारणा को पेश करने से पहले दाढ़ द्रव्यमान और मोल संख्याआइए इस संदर्भ में कुछ महत्वपूर्ण परिभाषाओं को देखें:
→ मोलर टर्म
मोलर शब्द से आया है अणु, लेकिन वास्तव में एक अणु क्या है? यह परमाणुओं का समूह है जो रासायनिक बंधों से जुड़े होते हैं।
→ आणविक द्रव्यमान (एमएम)
अणु के द्रव्यमान की गणना प्रत्येक परमाणु के परमाणु द्रव्यमान के योग से की जा सकती है जो संबंधित अणु को बनाता है। परिणाम को आणविक द्रव्यमान (MM) कहा जाता है।
हाइड्रोजन सल्फाइड का आणविक द्रव्यमान क्या होगा (H2एस) उदाहरण के लिए?
सबसे पहले आपको यह जानना होगा कि परमाणु भार प्रत्येक परमाणु का, जो कि आवर्त सारणी द्वारा दिया गया है तत्वों.
हाइड्रोजन का परमाणु द्रव्यमान (H) = 1 a.m.u. (परमाणु द्रव्यमान प्रति इकाई)
सल्फर का परमाणु द्रव्यमान (S) = 32.1 a.u.u.
आणविक द्रव्यमान परमाणुओं के परमाणु द्रव्यमान का योग है।
नोट: एच अणु का हाइड्रोजन2S का गुणांक 2 है, इसलिए आपको इसके द्रव्यमान को 2 से गुणा करना होगा। गणना करना:
H. का आण्विक द्रव्यमान2एस = 1 • 2 + 32.1 = 34.1 यू
(एच) + (एस) = (एच)2एस)
दाढ़ द्रव्यमान और मोल्स की संख्या
अब मत रोको... विज्ञापन के बाद और भी बहुत कुछ है;)
दाढ़ द्रव्यमान, साथ ही मोल्स की संख्या, से संबंधित है अवोगाद्रो का कॉन्स्टेंट (6.02 x 10 .)23) निम्नलिखित अवधारणा के माध्यम से:
''1 मोल में निहित प्राथमिक तत्वों की संख्या अवोगाद्रो स्थिरांक से मेल खाती है, जिसका मान 6.02 x 10 है।23 मोल-1.''
इसलिए, मोलर द्रव्यमान 6.02 x 10. का द्रव्यमान है23 रासायनिक संस्थाओं और g/mol में व्यक्त किया जाता है।
माइंड मैप - मोली
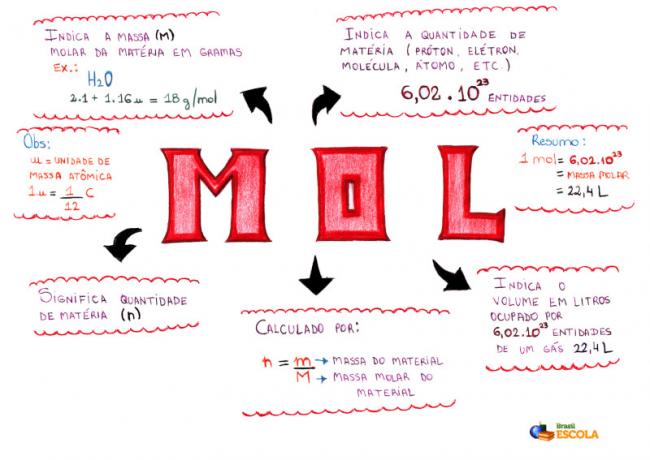
* माइंड मैप डाउनलोड करने के लिए, यहाँ क्लिक करें!
उदाहरण: एच2रों
आणविक द्रव्यमान = ३४.१ u
दाढ़ द्रव्यमान (M) = ३४.१ g/mol
इसका मतलब है कि, हाइड्रोजन सल्फाइड के ३४.१ ग्राम/मोल पर, हमारे पास ६.०२ x १०. है23 अणु या हाइड्रोजन सल्फाइड अणुओं का 1 मोल।
निष्कर्ष
आणविक द्रव्यमान और दाढ़ द्रव्यमान का मान समान होता है, माप की इकाई में अंतर होता है। मोलर द्रव्यमान मोल्स की संख्या से संबंधित होता है जो अवोगाद्रो स्थिरांक द्वारा दिया जाता है।
* मेरे द्वारा माइंड मैप। डिओगो लोपेज
लिरिया अल्वेस द्वारा
रसायन विज्ञान में स्नातक
क्या आप इस पाठ को किसी स्कूल या शैक्षणिक कार्य में संदर्भित करना चाहेंगे? देखो:
सूजा, लिरिया अल्वेस डी। "मोलर मास और मोल नंबर"; ब्राजील स्कूल. में उपलब्ध: https://brasilescola.uol.com.br/quimica/massa-molar-numero-mol.htm. 27 जून, 2021 को एक्सेस किया गया।