प्रतिवर्ती प्रतिक्रियाएं आमतौर पर एक निश्चित मात्रा में अभिकर्मकों से शुरू होती हैं। जैसे ही सीधी प्रतिक्रिया शुरू होती है, समय के साथ, इन अभिकर्मकों का निर्माण के लिए उपयोग किया जाता है उत्पादों की, फलस्वरूप अभिकर्मकों की सांद्रता घट जाती है जबकि उत्पादों की सांद्रता concentration बढ़ती है। फिर, प्रतिलोम प्रतिक्रिया भी शुरू हो जाती है, अभिकारकों का भी उत्पादन होता है, जब तक कि प्रत्यक्ष और प्रतिलोम प्रतिक्रियाओं के विकास की दर (गति) समान रहती है, तथाकथित तक पहुंच जाती है रासायनिक संतुलन.
संतुलन में, संतुलन स्थिरांक Kc होता है, जिसे मूल रूप से व्यक्त किया जाता है:
|
केसी = [उत्पाद]संतुलित रासायनिक समीकरण में गुणांक [अभिकर्मक]संतुलित रासायनिक समीकरण में गुणांक |
अर्थात्, निम्नलिखित सामान्य संतुलन प्रतिक्रिया पर विचार करना:
ए ए + बी बी ↔ सी सी + डी डी
चूंकि लोअरकेस अक्षर गुणांक हैं, और अपरकेस अक्षर पदार्थ हैं, इस प्रतिक्रिया का संतुलन स्थिरांक होगा:
केसी = [सी]सी. [डी]घ
[द]. [बी]ख
इसके बारे में अधिक विवरण पाठ में देखा जा सकता है Kc और Kp संतुलन स्थिरांक. यह पाठ हमें कुछ महत्वपूर्ण भी दिखाता है: कि केसी मूल्य हमें दिखा सकते हैं कि क्या अभिकर्मकों की एकाग्रता और उत्पाद समान हैं या यदि एक दूसरे से बड़ा है और, परिणामस्वरूप, यदि रासायनिक संतुलन किसी दिशा में स्थानांतरित हो जाता है प्रतिक्रिया।
इसलिए हमें Kc का मान ज्ञात करना होगा। ऐसा करने के लिए, याद रखें कि ये गणना प्रयोगात्मक हैं, तो आइए प्रतिक्रियाओं के कुछ उदाहरण और उनसे प्राप्त आंकड़ों को देखें।
कुछ ऐसा जो इन गणनाओं को करने में बहुत मददगार है, वह है नीचे दी गई तालिका के समान एक तालिका लिखना और उसमें बताए गए चरणों का पालन करना:

संतुलन स्थिरांक की गणना करने के लिए उपयोग किए गए डेटा को व्यवस्थित करने के लिए तालिका
अब, अभ्यास पर चलते हैं:
उदाहरण 1: एक बंद कंटेनर में, 2 एल की क्षमता के साथ, 100 डिग्री सेल्सियस के तापमान पर, एन. का 20 मोल होता है2हे4. निम्नलिखित प्रतिवर्ती प्रतिक्रिया होने लगती है: N2हे4 नहीं2. कुछ समय बाद, यह पाया गया कि प्रतिक्रिया रासायनिक संतुलन तक पहुँच गई और वह 8 mol NO2 गठन किया था। 100°C तापमान पर संतुलन स्थिरांक Kc का मान क्या है?
अब मत रोको... विज्ञापन के बाद और भी बहुत कुछ है;)
संकल्प:
आइए तालिका का उपयोग करें:

संतुलन स्थिरांक गणना उदाहरण को हल करने के लिए उपयोग की जाने वाली तालिका
ध्यान दें कि जिस पंक्ति में प्रतिक्रिया और रूप देने वाली मात्राएँ लिखी गई थीं, हम जानते हैं कि N के 4 मोल खर्च किए गए थे2हे4, क्योंकि अनुपात 1: 2 है, और यह कि 8 mol NO का गठन किया गया था2.
अब बस इस प्रतिक्रिया के संतुलन स्थिरांक Kc के व्यंजक में पाए गए मानों को बदलें:
केसी = [पर2]2
[एन2हे4]
केसी = (4 मोल / एल) 2
(8 मोल / एल)
केसी = 2 मोल/ली
Kc का मान विमाविहीन है, इसकी किसी परिमाण से संबंधित कोई इकाई नहीं है।
अब, आइए एक उदाहरण देखें, जिसमें शुरू से ही उत्पाद भी शामिल हैं:
उदाहरण 2: 5 L की क्षमता वाले एक बंद कंटेनर में, तापमान T पर 2 मोल हाइड्रोजन गैस, 3 मोल आयोडीन गैस और 4 मोल हाइड्रोजन आयोडाइड होते हैं। प्रतिक्रिया तापमान T पर रासायनिक संतुलन में प्रवेश करती है, और यह पता चलता है कि बर्तन में 1 मोल हाइड्रोजन गैस है। इस संतुलन का प्रतिनिधित्व करने वाला ग्राफ क्या है और T के तापमान पर संतुलन स्थिरांक Kc का मान क्या है?
संकल्प:
तालिका का उपयोग करना:
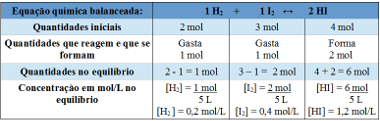
संतुलन स्थिरांक निर्धारित करने के लिए प्रयुक्त तालिका
अभिकर्मकों और उत्पादों के mol/L सांद्रता में भिन्नता दिखाने वाला ग्राफ जब तक वे संतुलन तक नहीं पहुँच जाते, तब तक दिया जा सकता है:

रासायनिक संतुलन ग्राफ अभिकर्मकों और उत्पादों की सांद्रता में परिवर्तन दिखा रहा है
अब हम संतुलन स्थिरांक का मान ज्ञात करते हैं:
केसी =__[HI]2__
[एच2 ]. [मैं2]
केसी = (1,2)2
0,2. 0,4
केसी = 18
जेनिफर फोगाका द्वारा
रसायन विज्ञान में स्नातक
क्या आप इस पाठ को किसी स्कूल या शैक्षणिक कार्य में संदर्भित करना चाहेंगे? देखो:
FOGAÇA, जेनिफर रोचा वर्गास। "संतुलन स्थिरांक Kc की गणना"; ब्राजील स्कूल. में उपलब्ध: https://brasilescola.uol.com.br/quimica/calculo-constante-equilibrio-kc.htm. 28 जून, 2021 को एक्सेस किया गया।
रसायन विज्ञान

रासायनिक संतुलन पर हल किए गए अभ्यासों की इस सूची के साथ अपने ज्ञान का परीक्षण करें और और जानें। इस सामग्री के माध्यम से, आप बेहतर ढंग से समझ पाएंगे कि संतुलन स्थिरांक (केपी, केसी और की), संतुलन शिफ्ट, पीएच और पीओएच, साथ ही तथाकथित बफर समाधानों में संतुलन कैसे काम करते हैं।