जब हम लौ की क्रिया के लिए अलग-अलग तत्व जमा करते हैं, तो हम देखते हैं कि प्रत्येक एक अलग रंग का उत्सर्जन करता है। उदाहरण के लिए, यदि हम एक स्ट्रोंटियम, एक सोडियम और एक तांबे का नमक जलाते हैं, तो हम क्रमशः लाल, तीव्र पीले और हरे रंग देखेंगे, जैसा कि निम्नलिखित आकृति में दिखाया गया है:

यदि इन ज्वालाओं का प्रकाश प्रिज्म पर पड़ता है, तो a असंतत स्पेक्ट्रम, अर्थात्, बिना प्रकाश वाले क्षेत्रों के साथ प्रतिच्छेदित केवल कुछ रंगीन चमकदार रेखाएं ही देखी जाएंगी। प्रत्येक तत्व के लिए, हमारे पास एक अलग स्पेक्ट्रम होगा।

इस प्रकार के स्पेक्ट्रा को कहा जाता है उत्सर्जन चित्र, क्योंकि वे एक निश्चित तत्व द्वारा जारी किए गए थे और इसकी पहचान करने के लिए काम करते हैं।
उच्च पर विद्युत निर्वहन ट्यूब में उत्पन्न प्रकाश किरण के माध्यम से इस तरह का स्पेक्ट्रा प्राप्त करना संभव है तापमान और कम दबाव, जिसमें कुछ तत्वों जैसे हाइड्रोजन, या महान गैसों से गैसें होती हैं बोले:

एक प्रिज्म के माध्यम से उत्पन्न इस विद्युत चुम्बकीय विकिरण (प्रकाश) को पारित करके, इनमें से प्रत्येक तत्व का उत्सर्जन स्पेक्ट्रा प्राप्त होता है।
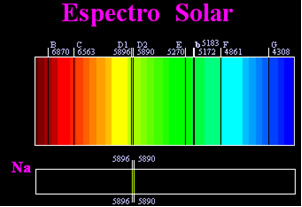
पहले, यह माना जाता था कि प्राप्त किया गया सौर स्पेक्ट्रम पूरी तरह से निरंतर था, लेकिन अंग्रेजी वैज्ञानिक विलियम हाइड वोलास्टन ने पाया कि प्रकाश की एक बहुत ही संकीर्ण किरण के साथ काम करते हुए, लगभग 0.01 मिमी की एक भट्ठा के साथ, आप देख सकते हैं कि सौर स्पेक्ट्रम में सात काली रेखाएँ हैं इसके बारे में। बाद में, युवा जोसेफ़ फ्रौनहोफ़रho (१७८७-१८२६) ने प्रिज्म और विवर्तन झंझरी का उपयोग करते हुए पाया कि सौर स्पेक्ट्रम में वास्तव में हजारों आरोपित काली रेखाएं हैं।
कुछ समय बाद भौतिक गुस्ताव रॉबर्ट किरचॉफ उन्होंने देखा कि सोडियम स्पेक्ट्रम द्वारा प्राप्त पीले धब्बे ठीक उसी स्थान पर थे जैसे सूर्य के स्पेक्ट्रम में दो काली रेखाएँ। वह और रसायनज्ञ रॉबर्ट विल्हेम बन्सेन कई प्रयोग किए और देखा कि अगर बन्सन बर्नर से एक सफेद रोशनी, जैसे सूरज की रोशनी, सोडियम द्वारा उत्सर्जित पीली रोशनी से गुजरती है और स्पेक्ट्रम उत्पन्न करने के लिए प्रिज्म को पार किया जाता है; परिणाम इंद्रधनुष के रंगों में एक सतत सौर स्पेक्ट्रम होगा, लेकिन सोडियम स्पेक्ट्रम में पीली रेखाओं के समान स्थिति में काली रेखाओं (जिसे फ्रौनहोफर द्वारा डी लाइन कहा जाता है) के साथ।
अब मत रोको... विज्ञापन के बाद और भी बहुत कुछ है;)
सूर्य लाल से लेकर बैंगनी तक सभी रंगों का प्रकाश उत्सर्जित करता है, हालांकि, पृथ्वी के वायुमंडल से गुजरते समय, मौजूद गैसें सूर्य के प्रकाश को ठीक उसी रंग में अवशोषित करती हैं, जैसा वे उत्सर्जित करती हैं।
इस प्रकार के स्पेक्ट्रा को कहा जाता है अवशोषण स्पेक्ट्रा.
इन टिप्पणियों के आधार पर, Kirchhoff तीन बनाया कानून स्पेक्ट्रोस्कोपी के लिए, जो हैं:
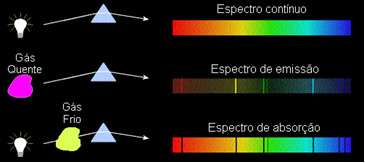
१) एक शरीर न झिल्लड़ गर्म, तीन भौतिक अवस्थाओं में से किसी में, एक स्पेक्ट्रम उत्सर्जित करता है निरंतर.
2) एक गैस पारदर्शक - उन महान गैसों की तरह जिन्हें हमने ऊपर देखा - एक. पैदा करता है उत्सर्जन चित्र, की उपस्थिति के साथ पंक्तियां उज्ज्वल। इन रेखाओं की संख्या और स्थिति गैस में मौजूद रासायनिक तत्वों द्वारा निर्धारित की जाएगी।
3) यदि ए If निरंतर स्पेक्ट्रम एक गैस से गुजरता है न्यूनतम तापमान पर, ठंडी गैस किसकी उपस्थिति का कारण बनती है? काली रेखाएं, यह है अवशोषण स्पेक्ट्रम. सोडियम गैस से गुजरने वाले सूर्य के प्रकाश के स्पेक्ट्रम के साथ यही हुआ। इस मामले में, अवशोषण स्पेक्ट्रम में रेखाओं की संख्या और स्थिति भी गैस में मौजूद रासायनिक तत्वों पर निर्भर करती है।
जेनिफर फोगाका द्वारा
रसायन विज्ञान में स्नातक
क्या आप इस पाठ को किसी स्कूल या शैक्षणिक कार्य में संदर्भित करना चाहेंगे? देखो:
FOGAÇA, जेनिफर रोचा वर्गास। "उत्सर्जन और अवशोषण स्पेक्ट्रा और किरचॉफ के नियम"; ब्राजील स्कूल. में उपलब्ध: https://brasilescola.uol.com.br/quimica/espectros-emissao-absorcao-leis-kirchhoff.htm. 27 जून, 2021 को एक्सेस किया गया।



