हे की गणना परमाणु भार एक तत्व का गणितीय संसाधन है जिसका उपयोग मौजूदा रासायनिक तत्वों में से प्रत्येक की आवर्त सारणी में मौजूद द्रव्यमान मूल्य को निर्धारित करने के लिए किया जाता है। सामान्य तौर पर, carry को पूरा करने के लिए परमाणु द्रव्यमान गणना, हमें निम्नलिखित चरों को जानना चाहिए: रासायनिक तत्व:
तत्व समस्थानिक;
तत्व के प्रत्येक समस्थानिक की द्रव्यमान संख्या;
प्रकृति में तत्व के प्रत्येक समस्थानिक का प्रतिशत।
उदाहरण के लिए, हाइड्रोजन के परमाणु द्रव्यमान की गणना निम्नलिखित आंकड़ों के आधार पर की गई थी:
प्रोटियम समस्थानिक प्रस्तुत करता है (H1), ड्यूटेरियम (H .)2) और ट्रिटियम (H .)3);
इन समस्थानिकों का द्रव्यमान क्रमशः 1, 2 और 3 है;
प्रकृति में प्रोटियम का प्रतिशत 98.9% है;
प्रकृति में ड्यूटेरियम का प्रतिशत 0.09% है;
प्रकृति में ट्रिटियम का प्रतिशत 0.01% है।
अब मत रोको... विज्ञापन के बाद और भी बहुत कुछ है;)
परमाणु द्रव्यमान की गणना के लिए गणितीय मानक
को अंजाम देने के लिए परमाणु द्रव्यमान गणना किसी भी रासायनिक तत्व के लिए, हमें निम्नलिखित गणितीय पैटर्न का उपयोग करना चाहिए:
1हे: प्रत्येक समस्थानिक की द्रव्यमान संख्या को उसके प्रतिशत से गुणा करें;
2हे: पहले चरण के गुणन में पाए गए सभी परिणाम जोड़ें;
3हे: पाई गई राशि को 100 से विभाजित करें।
एमए = द्रव्यमान संख्या.प्रतिशत + द्रव्यमान संख्या.प्रतिशत
100
माइंड मैप: परमाणु द्रव्यमान
*मानसिक मानचित्र को PDF में डाउनलोड करने के लिए, यहाँ क्लिक करें!
परमाणु द्रव्यमान गणना के उदाहरण
पहला उदाहरण: सल्फर के परमाणु द्रव्यमान की गणना।
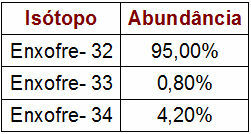
सल्फर आइसोटोप का प्रतिशत और मास डेटा Mass
प्रदान की गई तालिका प्रकृति में प्रत्येक सल्फर समस्थानिक की द्रव्यमान संख्या और प्रतिशत दर्शाती है। परमाणु द्रव्यमान की गणना करने के लिए, बस निम्नलिखित चरणों का पालन करें:
1हे चरण: प्रत्येक समस्थानिक की द्रव्यमान संख्या को उसकी बहुतायत के मान से गुणा करें।
सल्फर - 32 (S32)
रों32 = 32.95
रों32 = 3040
सल्फर - 33 (S (33)
रों33 = 33.0,8
रों33 = 26,4
सल्फर - 34 (S (34)
रों34 = 34.4,2
रों34 = 142,8
2हे चरण: द्रव्यमान संख्या के गुणन और समस्थानिक की प्रचुरता में पाए जाने वाले मानों को जोड़ें।
योग = एस32 + एस33 + एस34
योग = 3040 + 26.4 + 142.8
योग = ३२०९.२
3हे चरण: 100 से प्राप्त परिणामों के योग को विभाजित करके परमाणु द्रव्यमान की गणना करें:
एमए = योग
100
एमए = 3209,2
100
एमए = 32.092 यू
दूसरा उदाहरण: किसी दिए गए रासायनिक तत्व (D) में तीन समस्थानिक होते हैं, जिनकी द्रव्यमान संख्याएँ हैं:
30घ 32घ 34घ
यह जानते हुए कि इस तत्व का परमाणु द्रव्यमान 32.20 u है और समस्थानिक का 20% है 32डी प्रकृति में, अन्य समस्थानिकों के प्रतिशत का मान क्या है?
कथन द्रव्यमान संख्या, परमाणु द्रव्यमान और समस्थानिकों में से एक का प्रतिशत देता है। अन्य समस्थानिकों का प्रतिशत निर्धारित करने के लिए, हमें निम्नलिखित चरणों का पालन करना चाहिए:
1हे चरण: प्रत्येक आइसोटोप का प्रतिशत निर्धारित करें।
आइसोटोप - 30 (डीएस .)30)
डी एस30 = 30.x
डी एस30 = 30x
आइसोटोप - 32 (डीएस .)32)
डी एस32 = 32.20
डी एस32 = 640
आइसोटोप - 34 (डी .)34)
डी एस34 = 34.y
डी एस34 = ३४ वर्ष
2हे चरण: परमाणु द्रव्यमान की गणना के लिए गणितीय अभिव्यक्ति में पाए गए सभी डेटा का उपयोग करें।
एमए = द्रव्यमान संख्या.प्रतिशत + द्रव्यमान संख्या.प्रतिशत
100
32,2 = 30x + 640 + 34y
100
32,2.100 = 30x + 640 + 34y
100
3220 - 640 = 30x+34y
30x + 34y = 2580
एक्स = २५८० - ३४ वर्ष
30
3हे चरण: निम्नलिखित तर्क से ऊपर पाए गए अभिव्यक्ति का प्रयोग करें:
आइसोटोप 1 का प्रतिशत + आइसोटोप 2 का प्रतिशत + आइसोटोप 3 का प्रतिशत = 100%
एक्स + 20 + वाई = 100
एक्स + वाई = 100 - 20
एक्स + वाई = 80
एक्स = 80 - वाई
२५८० - ३४ वर्ष = 80-y
30
2580 - 34y = 30। (८०-वाई)
२५८०- ३४ y = २४०० - ३०y
2580 - 2400 = 34y-30y
4y = 180
वाई = 80
4
वाई = 45%
4हे चरण: तीसरे चरण में निर्मित व्यंजक में x के प्रतिशत मान की गणना कीजिए।
एक्स + वाई = 80
एक्स + 45 = 80
एक्स = 80 - 45
एक्स = ३५%
मेरे द्वारा। डिओगो लोपेज डायस
क्या आप इस पाठ को किसी स्कूल या शैक्षणिक कार्य में संदर्भित करना चाहेंगे? देखो:
DAYS, डिओगो लोपेज। "परमाणु द्रव्यमान गणना"; ब्राजील स्कूल. में उपलब्ध: https://brasilescola.uol.com.br/quimica/calculo-massa-atomica.htm. 27 जून, 2021 को एक्सेस किया गया।


