परमाणु असीम रूप से छोटे कण होते हैं जो ब्रह्मांड में सभी पदार्थों को बनाते हैं। समय के साथ, वैज्ञानिकों द्वारा की गई नई खोजों के अनुसार परमाणु संरचना कैसी होगी, इसका विचार बदल गया। आप इसके बारे में पाठ में अधिक जानकारी प्राप्त कर सकते हैंपरमाणु मॉडल का विकास.
एक मॉडल वास्तविकता का प्रतिनिधित्व है (वास्तविकता स्वयं नहीं), इसलिए परमाणु मॉडल का प्रतिनिधित्व करते हैं परमाणु के मुख्य घटक और इसकी संरचना और पदार्थ के कुछ भौतिक और रासायनिक व्यवहार की व्याख्या करते हैं। ऐसा इसलिए किया जाता है क्योंकि एक इंसान के लिए अल्ट्रामाइक्रोस्कोप से भी एक अलग परमाणु को देखना अभी तक संभव नहीं है।
परमाणु कितना छोटा है इसका अंदाजा लगाने के लिए जानिए एक साधारण सूक्ष्मदर्शी से दिखाई देने वाले सबसे छोटे कण में दस अरब से अधिक परमाणु होते हैं! परमाणु इतना छोटा है कि, अगर हम उनमें से एक लाख को एक साथ रख दें, तो हम उस तक नहीं पहुंच पाएंगे एक बाल की मोटाई।
माइंड मैप: परमाणु
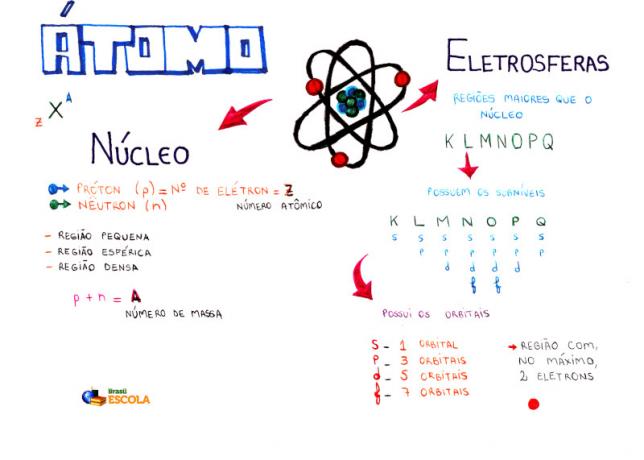
* माइंड मैप को पीडीएफ में डाउनलोड करने के लिए, यहाँ क्लिक करें!
परमाणु मॉडल में, परमाणु की संरचना और उसके गुणों को समझने के लिए वर्तमान में हाई स्कूल में सबसे अधिक इस्तेमाल किया जाने वाला रदरफोर्ड-बोहर मॉडल है। इस मॉडल के अनुसार, परमाणु की संरचना में दो मुख्य भाग होते हैं:
कोर और यह इलेक्ट्रोस्फीयर.
परमाणु की संरचना के दो मुख्य भाग - इलेक्ट्रोस्फीयर और न्यूक्लियस
* कोर: परमाणु के मध्य भाग के रूप में गठित, यह अधिक द्रव्यमान के कणों द्वारा गठित होने के अलावा कॉम्पैक्ट, विशाल और बहुत घना है, जो प्रोटॉन और न्यूट्रॉन हैं।

परमाणु नाभिक बनाने वाले प्रोटॉन और न्यूट्रॉन का चित्रण
- प्रोटॉन: वे एक धनात्मक विद्युत आवेश वाले कण हैं (सापेक्ष आवेश = +1; कूलम्ब में आवेश (C) = +1.602। 10-19) और इसका सापेक्ष द्रव्यमान 1 के बराबर है।
तथ्य यह है कि प्रोटॉन नाभिक बनाते हैं और इसे एक समग्र सकारात्मक चार्ज देते हैं, इसकी खोज की गई थी यूजीन गोल्डस्टीन, 1886 में, क्रुक्स की शीशी में संशोधन और कुछ प्रयोगों के माध्यम से। उन्होंने देखा कि, बहुत अधिक वोल्टेज के तहत, उत्सर्जन दिखाई दिया (एनोड किरणें - गैस के परमाणुओं के अवशेष जो बल्ब के अंदर थे और जिनके इलेक्ट्रॉन विद्युत निर्वहन से फट गए थे)। बल्ब के बाहर विद्युत या चुंबकीय क्षेत्र रखने से ये किरणें ऋणात्मक ध्रुव की ओर विक्षेपित हो जाती थीं। इसका मतलब था कि सकारात्मक उप-परमाणु कण थे, जिन्हें प्रोटॉन कहा जाता था।
बाद में, अर्नेस्ट रदरफोर्ड (१८७१-१९३७) ने पाठ में वर्णित प्रयोग किया रदरफोर्ड का परमाणु, जिसने उन्हें प्रोटॉन के स्थान की खोज करने के लिए प्रेरित किया: नाभिक में।
- न्यूट्रॉन: वे प्रोटॉन (1) के बराबर द्रव्यमान वाले कण होते हैं, लेकिन जैसा कि नाम से ही स्पष्ट है, वे तटस्थ हैं, अर्थात उनके पास विद्युत आवेश नहीं है।
1932 में न्यूट्रॉन की खोज की गई थी जेम्स चैडविक (१८९१-१९७४), जिन्होंने महसूस किया कि रेडियोधर्मी बेरिलियम के नाभिक प्रोटॉन के द्रव्यमान के बराबर द्रव्यमान वाले तटस्थ कणों का उत्सर्जन करते हैं (वास्तव में, यह थोड़ा बड़ा है)।
अब मत रोको... विज्ञापन के बाद और भी बहुत कुछ है;)
नाभिक का व्यास परमाणु के पास मौजूद प्रोटॉन और न्यूट्रॉन की मात्रा पर निर्भर करता है, लेकिन औसतन, यह लगभग 10 है।-14 महीना 10-15 म।
परमाणु नाभिक व्यावहारिक रूप से परमाणु के पूरे द्रव्यमान को एक बहुत छोटा हिस्सा होने के कारण केंद्रित करता है: प्रोटॉन और न्यूट्रॉन दोनों ही पूरे परमाणु से लगभग 100,000 गुना छोटे हैं! तुलना करके, कल्पना कीजिए कि हम तत्व हाइड्रोजन (जिसमें केवल. है) के परमाणु के नाभिक को बड़ा करते हैं एक प्रोटॉन) एक टेनिस गेंद के आकार के लिए, निकटतम इलेक्ट्रॉन. से लगभग तीन किलोमीटर की दूरी पर होगा दूरी! अगर एक परमाणु को 14 मंजिला इमारत की ऊंचाई तक बढ़ा दिया जाए, तो भी उसका कोर सातवीं मंजिल पर नमक के एक दाने के आकार का होगा। यह वास्तव में कुछ आश्चर्यजनक है, क्या आपको नहीं लगता?!
* इलेक्ट्रोस्फीयर: है वह क्षेत्र जहाँ इलेक्ट्रॉन नाभिक के चारों ओर घूम रहे हैं. नाभिक की तुलना में बहुत अधिक मात्रा का क्षेत्र होने के बावजूद, यह व्यावहारिक रूप से खाली है, क्योंकि प्रत्येक इलेक्ट्रॉन 1 प्रोटॉन (या 1 न्यूट्रॉन से) से 1836 गुना छोटा है। इसलिए परमाणु का द्रव्यमान व्यावहारिक रूप से नाभिक में ही होता है। इलेक्ट्रॉन एक ऋणात्मक विद्युत आवेश (-1) वाले कण होते हैं।
इलेक्ट्रान की खोज 1897 में ने की थी जोसेफ जॉन थॉमसन (१८५६-१९४०), के निर्माता थॉमसन परमाणु मॉडल. थॉमसन के प्रयोग को पाठ में विस्तार से देखा जा सकता है विद्युत निर्वहन के साथ थॉमसन का प्रयोग, लेकिन संक्षेप में, उन्होंने उपरोक्त क्रुक्स ampoule का उपयोग किया और महसूस किया कि कैथोड किरणें हमेशा होती हैं सकारात्मक ध्रुव द्वारा आकर्षित, जिसने साबित किया कि परमाणु में नकारात्मक कण थे, जिन्हें कहा जाता था इलेक्ट्रॉन।
इलेक्ट्रॉन एक सेकंड के प्रति दस लाखवें हिस्से में अरबों बार नाभिक के चारों ओर घूमते हैं, परमाणु को आकार देते हैं और ऐसा व्यवहार करते हैं जैसे कि यह ठोस हो।
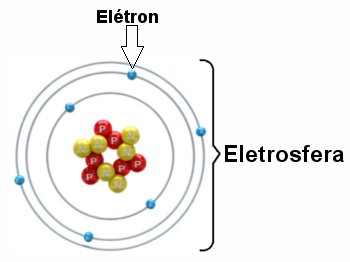
तीन इलेक्ट्रॉनिक परतों और नाभिक के चारों ओर घूमने वाले इलेक्ट्रॉनों के साथ एक इलेक्ट्रोस्फीयर का चित्रण।
संक्षेप में, हम तीन मुख्य उप-परमाणु कणों में अंतर करने के लिए एक तालिका बना सकते हैं जो परमाणु की संरचना का हिस्सा हैं:

तीन मुख्य उप-परमाणु कणों का द्रव्यमान और विद्युत आवेश - प्रोटॉन, न्यूट्रॉन और इलेक्ट्रॉन
सभी रासायनिक तत्वों के परमाणु इन तीन उप-परमाणु कणों से बने होते हैं। एक रासायनिक तत्व को दूसरे से जो अलग करता है वह वह मात्रा है जिसमें ये कण दिखाई देते हैं, विशेष रूप से नाभिक में प्रोटॉन की मात्रा, जिसे परमाणु संख्या कहा जाता है। पाठ के माध्यम से इसके बारे में अध्ययन करते रहें। रासायनिक तत्व.
* मेरे द्वारा माइंड मैप। डिओगो लोपेज
जेनिफर फोगाका द्वारा
रसायन विज्ञान में स्नातक
रसायन विज्ञान
पदार्थ, पानी, हाइड्रोसायनिक गैस, कार्बन डाइऑक्साइड, अमोनिया, हाइड्रोजन, हीलियम, पदार्थों का वर्गीकरण सरल, यौगिक पदार्थ, मिश्रण, मिश्रण के चरण, सजातीय मिश्रण, मिश्रण विषम।