आप एल्डीहाइड और यह कीटोन्स वे बहुत समान कार्बनिक कार्य हैं। दोनों की संरचना में कार्बोनिल कार्यात्मक समूह (C = O) होता है, केवल अंतर के साथ, के मामले में एल्डिहाइड, यह हमेशा कार्बन श्रृंखला के अंत में दिखाई देता है, अर्थात कार्बोनिल कार्बन लिगेंड्स में से एक है हाइड्रोजन; कीटोन्स में दो अन्य कार्बन परमाणुओं के बीच कार्बोनिल होता है।
एल्डिहाइड कार्यात्मक समूह:कीटोन्स का कार्यात्मक समूह:
हे हे
║ ║
सी सी एच सी सी सी
इस कारण से, एल्डिहाइड और कीटोन्स के बीच कार्यात्मक समरूपता के मामले हैं। उदाहरण के लिए, नीचे हम दो कार्यात्मक समावयवों को प्रस्तुत करते हैं जिनका आणविक सूत्र समान होता है (C .)3एच6ओ), लेकिन एक एल्डिहाइड (प्रोपेनल) है और दूसरा कीटोन (प्रोपेनोन) है। देखें कि यह कैसे उनके गुणों और अनुप्रयोगों को पूरी तरह से बदल देता है:
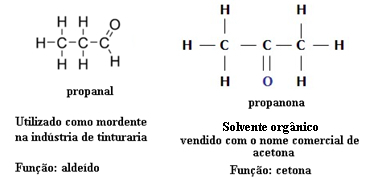
एल्डिहाइड और कीटोन के बीच फंक्शन आइसोमेरिज्म का उदाहरण
कल्पना कीजिए कि आप एक प्रयोगशाला में हैं और आपको एक रंगहीन तरल के साथ एक शीशी मिलती है जिसमें केवल आणविक सूत्र C होता है3एच6ओ यह पता लगाने के लिए आप क्या करेंगे कि यह कीटोन है या एल्डिहाइड?
इस तरह की समस्याओं को हल करने के लिए,
कमजोर ऑक्सीकरण एजेंटों के खिलाफ इन यौगिकों की प्रतिक्रिया के आधार पर एल्डिहाइड और कीटोन को अलग करने के तरीके हैं. जैसा कि नीचे दिया गया है, जब कमजोर ऑक्सीडेंट का सामना करना पड़ता है, तो एल्डिहाइड ऑक्सीकरण करके प्रतिक्रिया करते हैं, जबकि केटोन प्रतिक्रिया नहीं करते हैं। हम कहते हैं किएल्डिहाइड अपचायक के रूप में कार्य करते हैं, लेकिन कीटोन नहीं करते हैं, वे केवल ऊर्जावान ऑक्सीडेंट के संपर्क में कम करने वाले एजेंटों के रूप में प्रतिक्रिया करते हैं।एल्डिहाइड + कमजोर ऑक्सीडाइज़र → कार्बोक्जिलिक एसिड
ओ ओ
║ ║
सी ─ सी ─ एच + [ओ] → सी ─ सी ─ ओएच
केटोन्स + कमजोर ऑक्सीडाइज़र → प्रतिक्रिया न करें
हे
║
सी सी ─ सी + [ओ] → कोई प्रतिक्रिया नहीं होती है
उसके आधार पर, यह प्रतिक्रिया करने के लिए पर्याप्त है और देखें कि यौगिक प्रतिक्रिया करता है या नहीं। यदि यह प्रतिक्रिया करता है, तो हम जानते हैं कि यह एल्डिहाइड है; अगर यह प्रतिक्रिया नहीं करता है, तो यह कीटोन है।
इसके अलावा, इन एल्डिहाइड ऑक्सीकरण प्रतिक्रियाओं में बनने वाले उत्पाद काफी दिखाई देते हैं, जिसमें रंग परिवर्तन होते हैं, जैसा कि बाद में दिखाया जाएगा।
एल्डिहाइड और कीटोन में अंतर करने की तीन मुख्य विधियाँ हैं, जो हैं:
1- टोलेंस प्रतिक्रियाशील: यह अभिकर्मक है a सिल्वर नाइट्रेट का अमोनिया घोल, यानी इसमें सिल्वर नाइट्रेट (AgNO .) होता है3) और अतिरिक्त अमोनियम हाइड्रॉक्साइड (NH .)4ओह):
अग्नि3 + 3 एनएच4ओह → एजी (एनएच3) ओह + एनएच4पर3 + 2 एच2हे
टॉलेंस रिएक्टिव (जर्मन रसायनज्ञ बर्नहार्ड टॉलेंस (1841-1918) के नाम पर)
जैसा कि पाठ में बताया गया है चांदी का दर्पण बनाना, जब एक एल्डिहाइड को टोलेंस प्रतिक्रियाशील के संपर्क में लाया जाता है, तो यह संबंधित कार्बोक्जिलिक एसिड में ऑक्सीकृत हो जाता है, जबकि सिल्वर आयन एजी में कम हो जाते हैं0 (मेटालिक सिल्वर)। यदि यह प्रतिक्रिया की जाती है, उदाहरण के लिए, एक टेस्ट ट्यूब में, यह धातु चांदी ट्यूब की दीवारों पर जमा हो जाएगी, जिसके परिणामस्वरूप एक फिल्म बन जाएगी जिसे ए कहा जाता है। चांदी का दर्पण. यह देखा गया परिणाम बहुत सुंदर है और इसका उपयोग औद्योगिक दर्पण निर्माण प्रक्रिया में किया जाता है।
होने वाली प्रतिक्रिया को निम्नानुसार दर्शाया जा सकता है:
ओ ओ
║ ║
आर ─ सी ─ एच + एच2ओ → आर ─ सी ─ ओएच + 2e- + 2 एच+
२ एजी+ + 2e- → 2 Ag0
2 एनएच3 + 2 एच+ → 2 एनएच4+
हे हे
║║
आर सी एच + २ एजी+ + 2 एनएच3 +एच2हे → आर सी ओह + २ एजी0 + 2 एनएच4+
एल्डिहाइड टोलेंस प्रतिक्रियाशीलकार्बोज़ाइलिक तेजाब धातु चांदी (चांदी का दर्पण)
दूसरी ओर, यदि हम कीटोन को टॉलेंस प्रतिक्रियाशील के साथ प्रतिक्रिया करने के लिए डालते हैं, तो धात्विक चांदी का निर्माण नहीं होगा, क्योंकि केटोन्स Ag आयनों को कम नहीं कर सकते हैं।+.
2- फेलिंग रिएक्टिव: यह प्रतिक्रियाशील कॉपर सल्फेट II (CuSO .) का एक नीला घोल है4) एक मूल माध्यम में, क्योंकि यह सोडियम हाइड्रॉक्साइड (NaOH) और सोडियम और पोटेशियम टार्ट्रेट (NaOOC-CHOH-CHOH-COOK) द्वारा निर्मित एक अन्य घोल के साथ मिलाया जाता है। इसे स्थिर करने और इसकी वर्षा को रोकने के लिए कॉपर II सल्फेट के घोल में टार्ट्रेट मिलाया जाता है।
CUSO4 + 2 NaOH → Na2केवल4 + घन (ओएच)2
फेलिंग रिएक्टिव (जर्मन रसायनज्ञ हरमन वॉन फेहलिंग (1812-1885) के नाम पर)
फेहलिंग की प्रतिक्रियाशील के संपर्क में, एक एल्डिहाइड अपने ऑक्सीकरण द्वारा कार्बोक्जिलिक एसिड बनाता है, जबकि कॉपर आयन (Cu)2+) बीच में मौजूद कम हो जाते हैं, जिससे एक लाल-भूरे रंग का अवक्षेप (अधिक ईंट जैसा) बनता है, जो कि क्यूप्रस ऑक्साइड है। दूसरी ओर, केटोन्स प्रतिक्रिया नहीं करते हैं - क्योंकि वे Cu आयनों को कम नहीं कर सकते हैं2+.
ओ ओ
║ ║
आर ─ सी ─ एच + 2 घन (ओएच)2 → आर ─ सी ─ ओएच + नितंब2हे + 2 एच2हे
एल्डिहाइड लाल-भूरे रंग का अवक्षेप
3- बेनेडिक्ट की प्रतिक्रियाशील: यह प्रतिक्रियाशील कॉपर II सल्फेट (Cu (OH)) के घोल से भी बनता है2) एक मूल माध्यम में, लेकिन इसे सोडियम साइट्रेट के साथ मिलाया जाता है।
फेलिंग के अभिकर्मक की तरह, एल्डिहाइड और बेनेडिक्ट के अभिकर्मक के बीच प्रतिक्रिया के मामले में, तांबे के आयन भी होते हैं (Cu2+) माध्यम में मौजूद होते हैं जो कम हो जाते हैं और लाल क्यूप्रस ऑक्साइड बनाते हैं।
मूत्र में ग्लूकोज की उपस्थिति और सामग्री का पता लगाने के लिए परीक्षणों में इस अभिकर्मक का व्यापक रूप से उपयोग किया जाता है। ग्लूकोज की संरचना में एक एल्डिहाइड समूह होता है, इसलिए यह इन परीक्षणों के लिए स्ट्रिप्स में मौजूद बेनेडिक्ट के अभिकर्मक के साथ प्रतिक्रिया करता है। वहां से, रिबन के रंग की तुलना उत्पाद की पैकेजिंग पर स्केल के रंग से करें।

बेनेडिक्ट के अभिकर्मक का उपयोग मूत्र में ग्लूकोज सामग्री को निर्धारित करने के लिए किया जाता है।
जेनिफर फोगाका द्वारा
रसायन विज्ञान में स्नातक
स्रोत: ब्राजील स्कूल - https://brasilescola.uol.com.br/quimica/diferenciacao-aldeidos-cetonas.htm
