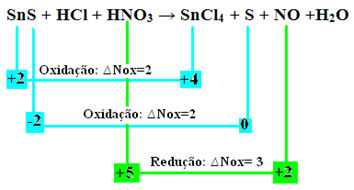
ऑक्सीकरण प्रतिक्रिया में, इलेक्ट्रॉनों का नुकसान होता है, जबकि कमी प्रतिक्रिया में इलेक्ट्रॉनों को प्राप्त करना होता है।
ऑक्सीकरण यह तीन परिस्थितियों में हो सकता है: जब पदार्थ में ऑक्सीजन मिलाया जाता है, जब कोई पदार्थ हाइड्रोजन खो देता है, या जब पदार्थ इलेक्ट्रॉनों को खो देता है। उदाहरण: फलों के सलाद हवा के संपर्क में आने पर काले पड़ जाते हैं, क्योंकि ऑक्सीजन फलों के ऑक्सीकरण को बढ़ावा देने का काम करती है। ऐसा न हो इसके लिए एक टिप नींबू या संतरे का रस मिलाना है, क्योंकि खट्टे फलों में मौजूद विटामिन सी सलाद पर ऑक्सीजन की ऑक्सीकरण क्रिया को रोकता है।
कमी, बदले में, विपरीत है और तीन तरीकों से भी होता है: जब कोई पदार्थ ऑक्सीजन खो देता है, जब वह हाइड्रोजन प्राप्त करता है, या जब वह इलेक्ट्रॉनों को प्राप्त करता है। उदाहरण: जब कॉपर ऑक्साइड (काला) को एक उपयुक्त उपकरण (कक्ष) में रखा जाता है, तो हाइड्रोजन गैस प्रवेश करती है। सुपर हीटेड कॉपर ऑक्साइड के संपर्क में आता है और परिणामस्वरूप यह ऑक्सीजन खो देता है और धीरे-धीरे गुलाबी हो जाता है क्योंकि इसे कम किया जा रहा है तांबा
ऑक्साइड-कमी प्रतिक्रिया: यह ज्ञात है कि एक ही रासायनिक प्रतिक्रिया में ऑक्सीकरण और कमी एक साथ होती है। इस घटना को कहा जाता है
इनमें से कुछ प्रतिक्रियाएं उद्योग के लिए बहुत उपयोगी हैं। उदाहरण के लिए, लौह अयस्क को कार्बन मोनोऑक्साइड (CO) के साथ ब्लास्ट फर्नेस में मिलाकर निकाला जाता है। इस प्रतिक्रिया में, अयस्क आयरन (Fe) बनाने के लिए ऑक्सीजन खो देता है और CO को CO. बनाने के लिए ऑक्सीजन प्राप्त करता है2 (कार्बन डाइऑक्साइड)। जंग एक रेडॉक्स प्रतिक्रिया के परिणामों में से एक है, जिसमें आयरन आयरन ऑक्साइड (जंग) बनाने के लिए ऑक्सीकरण करता है, और हवा में ऑक्सीजन कम हो जाता है।
रेडॉक्स प्रतिक्रिया का एक अन्य उदाहरण हवा के संपर्क में चांदी का है। चांदी की वस्तुएं समय के साथ अपनी चमकदार उपस्थिति खो देती हैं, सुस्त और गहरे रंग की हो जाती हैं। यह तथ्य इसलिए होता है क्योंकि वस्तु की सतह पर चांदी के परमाणु ऑक्सीजन जैसे अन्य पदार्थों के साथ प्रतिक्रिया करते हैं। फिर हम कहते हैं कि चांदी का ऑक्सीकरण हो गया है, अर्थात इसकी ऑक्सीकरण-कमी प्रतिक्रिया हुई है।
अब मत रोको... विज्ञापन के बाद और भी बहुत कुछ है;)
लिरिया अल्वेस द्वारा
रसायन विज्ञान में स्नातक
क्या आप इस पाठ को किसी स्कूल या शैक्षणिक कार्य में संदर्भित करना चाहेंगे? देखो:
सूजा, लिरिया अल्वेस डी। "ऑक्सीकरण और कमी"; ब्राजील स्कूल. में उपलब्ध: https://brasilescola.uol.com.br/quimica/oxidacao-reducao.htm. 27 जून, 2021 को एक्सेस किया गया।