भौतिक रसायन विज्ञान में मुख्य रूप से अध्ययन की जाने वाली ऑक्सीकरण-कमी प्रतिक्रियाएं वे हैं जिनमें इलेक्ट्रॉन स्थानांतरण होता है। प्रतिक्रियाशील प्रजाति (परमाणु, आयन या अणु) जो एक या एक से अधिक इलेक्ट्रॉनों को खोती है, वह है जो ऑक्सीकरण से गुजरती है। दूसरी ओर, इलेक्ट्रॉन प्राप्त करने वाली रासायनिक प्रजाति कम हो जाती है।
आम तौर पर, जब अकार्बनिक रसायन विज्ञान में इस प्रकार की प्रतिक्रिया का अध्ययन किया जाता है, तो इसे कहा जाता है सरल विनिमय प्रतिक्रिया या विस्थापन का।
किसी भी प्रतिक्रिया के होने के लिए कुछ शर्तों को पूरा करना आवश्यक है। उनमें से एक यह है कि वहाँ होना चाहिए रासायनिक आत्मीयता अभिकर्मकों के बीच, अर्थात्, उन्हें इस तरह से बातचीत करनी चाहिए कि नए पदार्थों के निर्माण को सक्षम किया जा सके।
रेडॉक्स प्रतिक्रियाओं के मामले में, आत्मीयता का मतलब है कि एक अभिकारक इलेक्ट्रॉनों को प्राप्त करने के लिए जाता है और दूसरा इलेक्ट्रॉनों को खो देता है। यह प्रवृत्ति से मेल खाती है जेट शामिल रासायनिक तत्वों की।
आइए देखें कि धातुओं के बीच प्रतिक्रियाशीलता की तुलना करना कैसे संभव है।
मान लें कि हम कॉपर II सल्फेट (CuSO .) के घोल को स्टोर करना चाहते हैं
4). हम इस विलयन को एल्युमीनियम के पात्र में नहीं रख सकते, क्योंकि निम्नलिखित अभिक्रिया होगी:२ अली(ओं) + 3 CuSO4(एक्यू)→ 3 Cu(ओं) + अली2(केवल4)3 (एक्यू)
ध्यान दें कि एल्यूमीनियम ऑक्सीकरण हो गया है, प्रत्येक में 3 इलेक्ट्रॉनों को खो रहा है और एल्यूमीनियम केशन बन गया है:
अली(ओं) → अल3+(यहां) + 3 और-
इसके साथ ही, धनायन तांबा (Cu2+) जो घोल में मौजूद था, एल्युमिनियम से इलेक्ट्रॉन प्राप्त करता था और कम होकर धात्विक तांबा बन जाता था। प्रत्येक तांबे के धनायन को दो इलेक्ट्रॉन प्राप्त होते हैं:
नितंब2+(यहां) + 2 और- → Cu(ओं)
हालांकि, अगर यह दूसरी तरफ था और हम एल्यूमीनियम सल्फेट (Al .) के समाधान को स्टोर करना चाहते थे2(केवल4)3 (एक्यू)), इसे तांबे के कंटेनर में रखने में कोई समस्या नहीं होगी, क्योंकि यह प्रतिक्रिया नहीं होगी:
नितंब(ओं) + अली2(केवल4)3 (एक्यू) → उत्पन्न नहीं होता
इन देखे गए तथ्यों को इस तथ्य से समझाया जा सकता है कि तांबे की तुलना में एल्यूमीनियम अधिक प्रतिक्रियाशील है more.
धातुओं में इलेक्ट्रॉनों को छोड़ने की प्रवृत्ति होती है, अर्थात ऑक्सीकरण करने के लिए। विभिन्न धातुओं की तुलना करते समय, इलेक्ट्रॉनों को दान करने की सबसे बड़ी प्रवृत्ति वाला सबसे अधिक प्रतिक्रियाशील होता है. नतीजतन, धातुओं की प्रतिक्रियाशीलता भी उनके साथ जुड़ी हुई है आयनीकरण ऊर्जा, अर्थात्, गैसीय परमाणु से उसकी जमीनी अवस्था में एक इलेक्ट्रॉन को निकालने के लिए आवश्यक न्यूनतम ऊर्जा।
अब मत रोको... विज्ञापन के बाद और भी बहुत कुछ है;)

इसके आधार पर, धातु प्रतिक्रियाशीलता कतार या इलेक्ट्रोलाइटिक वोल्टेज की पंक्ति, नीचे दिखाया गया है:
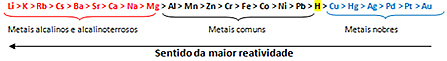
सबसे अधिक प्रतिक्रियाशील धातु उन आयनिक पदार्थों के साथ प्रतिक्रिया करती है जिनके धनायन कम प्रतिक्रियाशील होते हैं। दूसरे शब्दों में, बायीं ओर की धातु उसके दायीं ओर आयनों द्वारा निर्मित पदार्थ के साथ अभिक्रिया करती है। विपरीत नहीं होता है।
दिए गए उदाहरण को याद करते हुए, प्रतिक्रियाशीलता पंक्ति में देखें कि एल्यूमीनियम (Al) तांबे (Cu) के बाईं ओर है। इसलिए, एल्यूमीनियम तांबे के पिंजरों द्वारा गठित समाधान के साथ प्रतिक्रिया करता है; लेकिन कॉपर एल्युमिनियम के धनायनों द्वारा बनाए गए घोल के साथ प्रतिक्रिया नहीं करता है।
ध्यान दें कि सबसे अधिक प्रतिक्रियाशील धातु लिथियम (Li) है और सबसे कम प्रतिक्रियाशील सोना (Au) है।

यह एक कारण है कि सोना इतना मूल्यवान क्यों है, क्योंकि अगर यह प्रतिक्रिया नहीं करता है, तो यह लंबे समय तक बरकरार रहता है। यह सोने से लिपटे मिस्र के सरकोफेगी और मूर्तियों में देखा जा सकता है जो सबसे दूरस्थ पुरातनता की हैं। जब हम शुद्ध सोने के गहनों के स्थायित्व की तुलना अन्य धातुओं से बने गहनों से करते हैं जो सोने की तुलना में अधिक प्रतिक्रियाशील होते हैं, तो हम इसकी कल्पना भी करते हैं।

जेनिफर फोगाका द्वारा
रसायन विज्ञान में स्नातक
क्या आप इस पाठ को किसी स्कूल या शैक्षणिक कार्य में संदर्भित करना चाहेंगे? देखो:
FOGAÇA, जेनिफर रोचा वर्गास। "धातुओं की प्रतिक्रियाशीलता का क्रम"; ब्राजील स्कूल. में उपलब्ध: https://brasilescola.uol.com.br/quimica/ordem-reatividade-dos-metais.htm. 28 जून, 2021 को एक्सेस किया गया।



