la définition de matière est donnée par une phrase simple et complète: c'est tout ce qui occupe une place (le même que le volume) dans l'espace et a un poids (un produit de la masse et de la gravité). Quelques exemples de matière: arbre, bactérie, virus, être humain, air, eau, table, véhicule, etc.
On pourrait citer des milliers d'exemples, comme le matière c'est assez complet. Mais y a-t-il quelque chose qui n'a pas d'importance? Bien sûr, oui, cependant, dans ce cas, cela s'appelle énergie, comme dans les exemples suivants :
Lumière: appelée énergie lumineuse;
Pression: appelée énergie de pression;
Sonner: appelée énergie sonore;
Feu: association d'énergie thermique et lumineuse;
Électricité: appelé énergie électrique;
Chaleur: énergie thermique ;
Radiographie: une forme d'énergie électromagnétique;
LES énergie peut être défini comme un force capable de produire de l'action et du mouvement. Ainsi, il est très simple de différencier la matière de l'énergie, puisque l'une occupe de l'espace et a une masse, et l'autre pas.
Une curiosité importante pour le matière est qu'il peut être appelé de deux manières différentes: corps et objet.
Corps: c'est une partie du matière. Exemples: fil de laine, bris de verre, vent, tronc d'arbre ;
Objet: c'est une partie du matière qui a un usage particulier. Exemples: chemise, air comprimé, stylo, chaise.
Carte mentale: matière
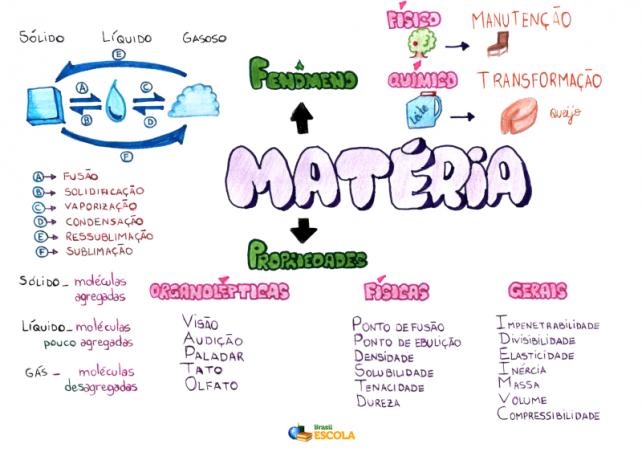
*Pour télécharger la carte mentale en PDF, Cliquez ici!
Composition de la matière
D'une manière générale, tous matière est formé par une unité structurelle de base, appelée atome, qui a la composition suivante :
Cœur: composé de protons et de neutrons;
protons: particules chargées positivement;
neutrons: particules non chargées;
Niveaux d'énergie: les régions où se trouvent les sous-niveaux ;
Sous-niveaux d'énergie : les régions où se trouvent les orbitales ;
Orbitales : les régions où les électrons sont les plus susceptibles de se trouver ;
électrons: particules chargées négativement.
Lorsque deux atomes ou plus se combinent, ils forment des molécules, qui peuvent former substances ainsi que des atomes isolés.
états physiques de la matière
Toi états physiques les plus courants dans lesquels nous pouvons trouver la matière sont:
Solide: état dans lequel les particules (atomes ou molécules), qui forment la matière, présentent le plus haut niveau d'organisation ;
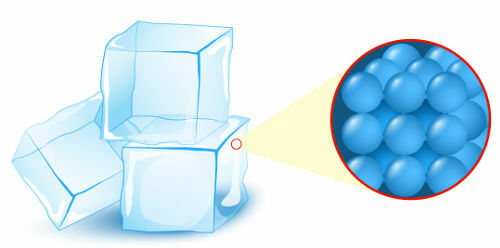
Représentation de l'organisation des particules à l'état solide
Liquide: état dans lequel les particules (atomes ou molécules), qui forment la matière, présentent un niveau d'organisation inférieur ;
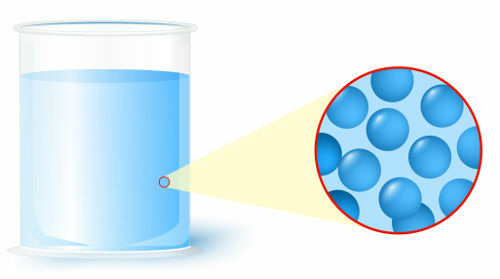
Représentation de l'organisation des particules à l'état liquide
Gazeux: un état dans lequel les particules (atomes ou molécules), qui forment la matière, n'ont aucune organisation.
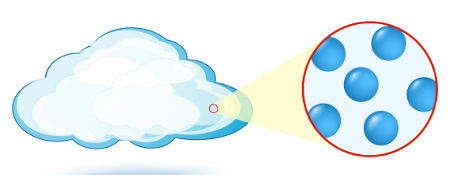
Représentation de l'organisation des particules à l'état gazeux
Propriétés générales de la matière
tout et tout matière, quel que soit le éléments chimiques qui le forment, doit avoir les propriétés spécifiées ci-dessous :
Élasticité: propriété que présente la matière à l'état solide lorsqu'elle est soumise à une force élastique extrême, sans que ses structures soient brisées. Lorsque cette force cesse, la matière revient à sa forme originelle ;
Compressibilité: lorsqu'une portion de matière à l'état gazeux est soumise à une compression, elle occupe un volume plus petit ;

Matériau comprimé dans un cylindre
Inertie: quand la matière est en mouvement, elle tend à rester en mouvement. S'il est au repos, la tendance est qu'il reste au repos ;
Divisibilité: la matière peut être décomposée en plus petites portions;
Impénétrabilité: deux sujets ne peuvent pas occuper le même espace en même temps.
Par moi Diogo Lopes Dias
La source: École du Brésil - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-materia.htm

