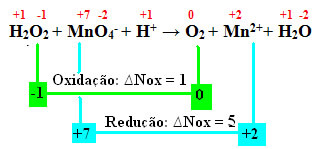
Les acides et les bases sont deux fonctions chimiques considérées comme opposées., c'est parce que leurs propriétés sont généralement inverses. Par exemple, si nous considérons les aliments présents dans notre vie quotidienne qui sont acides, nous verrons que leur goût, en général, est aigre, comme c'est le cas avec le citron. Cependant, les aliments basiques ont un goût astringent (qui « lie » la bouche), comme une banane verte.
Mais identifier une substance comme acide ou basique juste par goût, en plus d'être une méthode qui a de nombreuses chances d'échouer, il est également très dangereux car de nombreux acides et bases sont forts, toxiques et peuvent même tuer, comme l'acide. sulfurique (H2SEUL4), utilisé dans les batteries automobiles, et l'hydroxyde de sodium (NaOH), connu dans le commerce sous le nom de soude caustique.
Ainsi, les propriétés organoleptiques (propriétés qui concernent nos sens, telles que le goût et l'odorat) ne sont pas celles utilisées pour identifier les acides et les bases. Notez ci-dessous d'autres propriétés de ces fonctions organiques qui servent à les comparer et à les distinguer :
- Solubilité dans l'eau:
Toi acides être généralement bien soluble dans l'eau, tandis que la plupart socles é insoluble. Les bases de métaux alcalins sont solubles, les bases de métaux alcalino-terreux sont peu solubles et les bases d'autres métaux sont insolubles (une exception est l'hydroxyde d'ammonium, NH4OH, qui n'existe qu'en solution aqueuse, fait barboter le gaz ammoniac dans l'eau et y est donc soluble).
Quand on dit « insoluble », on veut dire que ces substances sont pratiquement insolubles, car aucune substance n'est totalement insoluble dans l'eau.
- Structure:
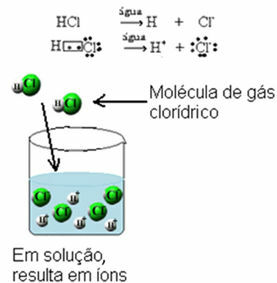
Tous les les acides sont moléculaires, c'est-à-dire formé par des liaisons covalentes dans lesquelles des électrons sont partagés. Un exemple est le gaz chlorhydrique, qui est formé en partageant une paire d'électrons entre l'hydrogène et le chlore :

déjà le les bases peuvent être ioniques ou moléculaires. Ceux qui contiennent des métaux alcalins et alcalino-terreux sont ioniques et les autres sont moléculaires.
Exemples:
NaOH: base ionique formée par les ions Na+ et oh-;
NH4OH: base moléculaire de l'ammoniac dans l'eau.
Ne vous arrêtez pas maintenant... Y'a plus après la pub ;)
- Conductivité électrique:
Tout les acides ne conduisent le courant électrique que lorsqu'ils sont dissous dans l'eau, car lorsqu'ils sont en milieu aqueux, ils subissent une ionisation, c'est-à-dire qu'ils libèrent des ions.
Exemple:
Tout les bases conduisent également le courant électrique en solution., comme les ioniques subissent une dissociation (libèrent les ions déjà existants dans la formule) et les moléculaires subissent une ionisation, réagissant avec l'eau et libérant des ions. À Les bases de métaux alcalins conduisent également le courant électrique lorsqu'elles sont à l'état liquide (fondu).
- Action sur les indicateurs:
Toi indicateurs acido-basiques sont des substances naturelles ou synthétiques qui subissent un changement de couleur lorsqu'elles entrent en contact avec un acide ou une base. Si un acide fait changer la couleur de l'indicateur, la base ramènera l'indicateur à sa couleur d'origine et vice versa.
Par exemple, la phénolphtaléine est un indicateur acido-basique très utilisé, et en milieu basique, elle devient d'un rose très intense; déjà en milieu acide, il devient incolore. Le papier de tournesol est également un bon indicateur, car dans un acide il devient rouge; et sur une base, il devient bleu.
Cela sert également à indiquer la différence de pH qui existe entre les acides et les bases.
- PH :
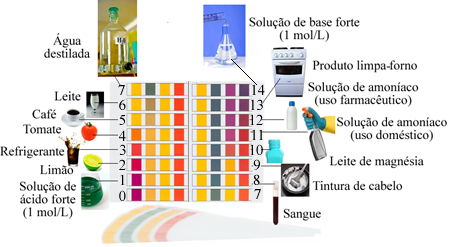
Un milieu considéré comme neutre a un pH égal à 7, comme c'est le cas de l'eau distillée.
Les acides ont un pH inférieur à 7, Pendant que les bases ont un pH supérieur à 7.
Exemples de solutions dont le pH est proche de celui indiqué par l'échelle :
- Action réciproque :
Lorsqu'ils sont mis en contact, les acides et les bases réagissent entre eux en se neutralisant, c'est-à-dire en rendant le pH du milieu neutre. C'est parce que le cation H+ de l'acide réagit avec l'anion OH- de la base, formant de l'eau. Ce type de réaction est appelé réaction de neutralisation et il produit aussi un sel.
Par Jennifer Fogaça
Diplômé en Chimie