Pour comprendre pourquoi quand on brûle du bois, il ne fond pas, rappelons d'abord ce qu'est une substance fondue, c'est-à-dire qu'elle est à l'état liquide.
La différence entre les états solide, liquide et gazeux réside uniquement dans l'état d'agrégation des particules. Dans les trois états, la substance est composée des mêmes particules, mais il y a plus ou moins d'espace entre elles.
A l'état solide, les particules sont plus rapprochées, sans grande liberté de mouvement. A l'état liquide, les particules ont plus de liberté et peuvent se déplacer.
Il s'avère qu'une grande partie du bois (50 %) est fabriquée à partir de cellulose, qui est en fait un polymère. Un polymère est formé par l'union de plusieurs molécules, appelées monomères. Dans le cas de la cellulose, elle est formée par l'union de centaines de molécules d'β-glucose, comme indiqué ci-dessous. La cellulose a alors la formule (C6H10O5)non et atteint des masses moléculaires de l'ordre de 400 000 u.
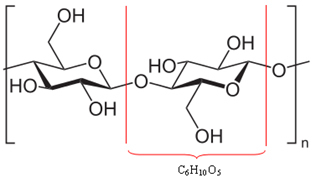
Comme ce sont de grosses molécules, ces polymères qui composent le bois ne peuvent pas se déplacer facilement. Notez également que les molécules d'β-glucose qui composent la cellulose ont des groupes hydroxyle (─ OH). Ces groupes lient l'hydrogène les uns aux autres, ce qui est le type de force intermoléculaire le plus intense, maintenant le polymère étroitement ensemble.

Liaisons hydrogène entre les molécules qui composent le polymère cellulosique*
Ainsi, pour rompre ces liens, il faudrait mettre tellement d'énergie dans le système que le bois se décompose avant même de fondre et n'est alors plus du bois.
Ainsi, lorsqu'il est brûlé, le bois subit une réaction chimique, qui est plus qu'un simple changement d'état physique. Ses molécules finissent par se décomposer et se recombiner avec l'oxygène présent dans l'air, formant alors de nouvelles substances, comme le gaz carbonique et l'eau.

* La source et auteur de l'image: laghi.l.
Par Jennifer Fogaça
Diplômé en Chimie
La source: École du Brésil - https://brasilescola.uol.com.br/quimica/por-que-madeira-nao-derrete.htm
