L'atome de carbone est considéré comme spécial pour sa capacité à former des liaisons avec d'autres atomes et à donner naissance à de longues chaînes carbonées. Tout est dû à la tétravalence du carbone, il peut se joindre en formant quatre liaisons, et les atomes participants peuvent être du carbone ou d'autres éléments. Ces derniers, lorsqu'ils sont présents dans la chaîne carbonée, sont appelés hétéroatomes.
Les hétéroatomes les plus courants sont: l'azote (N), l'oxygène, le soufre (S) et le phosphore (P).
Exemple:
L'atome d'oxygène présent dans la chaîne ci-dessus est un hétéroatome, car il est entre les carbones.
Mais méfiez-vous! Ne pas confondre la ramification avec le carbone hétéroatome, voir:
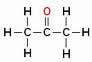
L'atome d'oxygène (en rouge) n'est pas situé entre les carbones mais au-dessus d'eux, formant une branche, il ne peut donc pas être considéré comme un hétéroatome.
Classification des atomes dans une chaîne carbonée:
Dans une chaîne, chaque carbone est classé en fonction du nombre d'autres atomes de carbone qui lui sont attachés.
carbone primaire: Directement attaché à seulement 1 autre carbone.
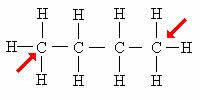
La flèche indique les carbones primaires. Notez que parce qu'ils sont situés aux extrémités de la chaîne carbonée, ces atomes se lient à seulement 1 carbone.
carbone secondaire: Directement lié à 2 autres carbones.

Les carbones indiqués sont situés entre deux carbones.
carbone tertiaire: Directement lié à 3 autres carbones.
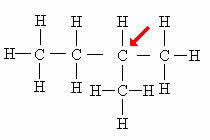
A noter que la présence de la branche (CH3) attaché à l'atome indiqué lui fait recevoir la classification de carbone tertiaire.
Carbone quaternaire: Directement lié à 4 autres carbones.
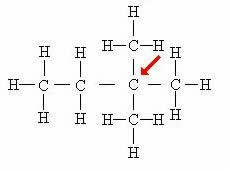
Dans ce cas, les quatre atomes attachés au carbone central (indiqué par la flèche) forment une sorte de « carré », ce qui témoigne encore plus de la présence du carbone quaternaire.
Par Líria Alves
Diplômé en Chimie
Équipe scolaire du Brésil
Voir plus!
Classification des chaînes carbonées: types de liaison
Propriétés des composés organiques
Chimie organique - Chimie - École du Brésil
La source: École du Brésil - https://brasilescola.uol.com.br/quimica/capacidade-compostos-organicos-formar-cadeias.htm


