Aussi bien que acides sulfoniques et les amines, les isonitriles sont des composés organiques issus de substances inorganiques, plus précisément d'un acide inorganique appelé acide isocyanhydrique.
Toi isonitriles ils sont largement utilisés dans diverses synthèses organiques (production de nouvelles substances organiques) et dans la fabrication de pesticides et de pesticides. Ces composés proviennent de la réaction de l'acide isocyanique avec un de l'alcool, par example. Dans cette réaction, l'atome d'hydrogène de l'acide est remplacé par le radical alcool. L'hydrogène rejoint l'hydroxyle de l'alcool et forme une molécule d'eau.
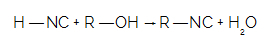
Lorsque HNC réagit avec un alcool, nous avons la formation d'isonitrile et d'une molécule d'eau
L'acide isocyanhydrique qui donne naissance aux isonitriles a la formule structurelle suivante :
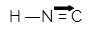
Entre l'atome de carbone et l'atome d'azote, il existe une double liaison et une liaison dative. Cette région de l'isonitrile est extrêmement polaire en raison du phénomène de résonance entre les électrons à double liaison et les électrons à liaison dative.
En raison de l'effet de résonance entre l'atome de carbone et d'azote, les isonitriles ont une plus faible stabilité par rapport aux nitriles, c'est-à-dire qu'ils peuvent se décomposer (se transformer en une autre substance) facilement. Ainsi, lorsqu'un isonitrile est chauffé, il se transforme facilement en un nitrile.
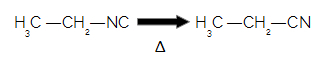
Lorsqu'on chauffe un isonitrile, il se transforme en nitrile
Quant aux caractéristiques physiques, les isonitriles :
sont moins denses que l'eau;
avoir des points de fusion et d'ébullition élevés par rapport aux substances de masse molaire approximative ;
Son état physique dépend de la taille de la masse molaire. Les isonitriles de masse molaire supérieure sont solides;
Ils sont peu solubles dans l'eau.
Pour effectuer le nomenclature d'un isonitrile, la règle de l'IUPAC (Union Internationale de Chimie Pure et Appliquée) est la suivante :
Nom de la branche + carbylamine
REMARQUE: Le nom carbylamine fait référence au groupe NC. Ainsi, tout groupe lié au NC est considéré comme un radical dans la nomenclature.
Voir quelques exemples :
Éthylcarbylamine: Isonitrile avec le radical éthyle

Vinylcarbylamine: Isonitrile avec le radical vinyle
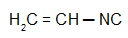
Isobutylcarbylamine: Isonitrile avec le radical isobutyle
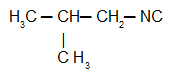
En plus de la nomenclature IUPAC, les isonitriles ont toujours la nomenclature habituelle, guidé par la règle suivante :
Isocyanure + de + nom radical + a
Isocyanure d'éthyle: Isonitrile avec le radical éthyle

Isocyanure de vinyle: Isonitrile avec le radical vinyle
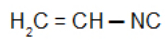
Isocyanure d'isobutyle: Isonitrile avec le radical isobutyle :
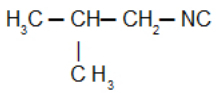
Par moi Diogo Lopes Dias

