Hybridation est le nom donné à la fusion ou à l'union d'orbitales atomiques incomplètes, phénomène qui augmente le nombre de des liaisons covalentes qu'un atome peut faire. Rappelons que l'orbitale est la région de l'atome où il y a une plus grande probabilité de trouver un électron.
Connaître le nombre de liaisons qu'un atome fait et comprendre le phénomène de hybridation, il est nécessaire de connaître quelques points fondamentaux sur l'atome :
1O point: les sous-niveaux d'énergie
Les sous-niveaux d'énergie qu'un atome peut avoir sont s, p, d, f.
2O point: nombre d'orbitales par sous-niveau
Chaque sous-niveau d'énergie a une quantité différente d'orbitales, comme nous pouvons le voir ci-dessous :
Sous-niveau s: 1 orbitale ;
sous-niveau p: 3 orbitales ;
Sous-niveau d: 5 orbitales.
La représentation générique de ces orbitales se fait comme suit :
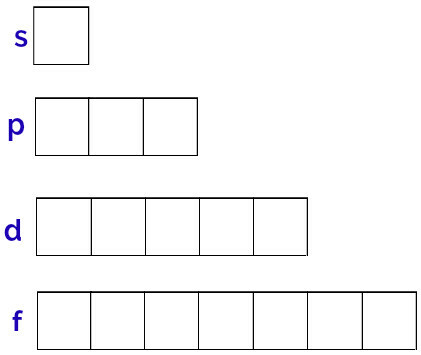
Représentation des orbitales de chaque sous-niveau
Selon Pauli, une orbitale peut avoir un maximum de 2 électrons, avec tourne (mouvements de rotation) opposés.
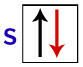
Représentation de l'orbitale s avec ses électrons
Selon Hund, une orbitale d'un sous-niveau ne reçoit son deuxième électron que lorsque toutes les autres orbitales de ce sous-niveau ont déjà reçu le premier électron.
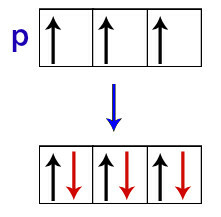
Distribution des électrons dans les orbitales de sous-niveau p
3O point: diffusion électronique
Pour comprendre l'hybridation et le nombre de liaisons que fait un atome, il est essentiel de réaliser le diffusion électronique sur le diagramme de Linus Pauling.

Diagramme de Linus Pauling
En rappelant que le nombre maximum d'électrons dans chaque sous-niveau est :
s = 2 électrons ;
p = 6 électrons ;
d = 10 électrons ;
f = 14 électrons.
Après cette brève revue, nous pouvons maintenant définir qu'est-ce que l'hybridation. Pour cela, nous utiliserons l'élément chimique bore (numéro atomique = 5) à titre d'exemple.
Lorsque nous effectuons une distribution électronique de bore, nous avons :
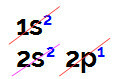
Distribution électronique du bore dans le diagramme de Linus Pauling
Il est possible d'observer dans cette distribution que le bore a 2 électrons dans le sous-niveau s et 1 électron dans le sous-niveau p de couche de valence.
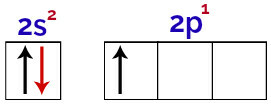
Électrons dans les orbitales de la couche de valence de bore
Comme le bore a 1 orbitale incomplète, il ne devrait donc faire qu'une seule liaison covalente, car le nombre de liaisons est toujours directement lié au nombre d'orbitales incomplètes.
Ainsi, lorsque l'atome de bore reçoit de l'énergie de l'environnement extérieur, ses électrons, en particulier ceux de la couche de valence, deviennent excités. Cela fait que l'un des électrons de l'orbitale s quitte et occupe l'une des orbitales p vides, résultant ainsi en 3 orbitales atomiques incomplètes, comme vous pouvez le voir sur l'image suivante :

Représentation de l'état excité de l'atome de bore
Enfin, il y a l'union de l'orbitale s incomplète avec les orbitales p incomplètes. Cette union s'appelle hybridation. Puisque nous avons la fusion d'une orbitale s avec deux p, on l'appelle hybridation sp2.
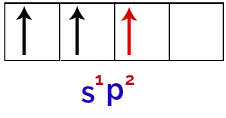
Représentation des orbitales hybridées dans l'atome de bore
Outre le bore, plusieurs autres éléments chimiques subissent le phénomène d'hybridation, comme le soufre (S), le Xénon (Xe), phosphore (P), carbone (Ç), béryllium (Être).
Par moi Diogo Lopes Dias
La source: École du Brésil - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-hibridizacao.htm
