Les carburants utilisés dans la plupart des voitures sont l'essence et l'éthanol. La combustion complète de ces deux carburants génère du dioxyde de carbone (CO2(g)) et de l'eau (H2O). Malheureusement, cependant, une combustion incomplète et les impuretés présentes dans l'alcool et l'essence peuvent générer des substances très polluantes pour l'environnement. Dans le cas de l'essence, le monoxyde de carbone (CO(g)); les hydrocarbures (composés constitués de carbone et d'hydrogène), tels que l'éthane (C2H6(g)); et oxydes d'azote (NOX), principalement le monoxyde d'azote (NO) et le dioxyde d'azote (NO2(g)).
Ainsi, pour éviter une augmentation de la pollution de l'air, toutes les voitures ont besoin d'équipements appelés pot catalytique ou pot catalytique, qui est un dispositif anti-pollution, qui a pour fonction de traiter ces gaz dégagés par le moteur à combustion interne et de les transformer en gaz moins nocifs. Les convertisseurs catalytiques sont également utilisés à cette fin dans certains processus industriels.
Les gaz polluants mentionnés sortent du moteur et pénètrent dans le pot catalytique en passant par une sorte de "ruche", dont les alvéoles sont généralement en matériau céramique ou métallique, qui est revêtu d'alumine (oxyde d'aluminium - Al2O3). Cette forme en nid d'abeille, avec de minuscules canaux, est importante car elle offre une grande surface de contact pour les gaz, les faisant réagir plus rapidement.
Mais le véritable catalyseur est un métal qui repose sur de l'oxyde d'aluminium. Typiquement, les métaux utilisés sont le palladium, le rhodium, le platine ou le molybdène. Vous pouvez également mélanger ces métaux et utiliser des alliages. Par exemple, dans le cas de l'essence, un alliage de palladium et de thorium est normalement utilisé; dans le cas de l'éthanol, un autre alliage de palladium et de molybdène est utilisé. Ces métaux effectuent une catalyse hétérogène avec des gaz polluants.
catalyse hétérogène c'est un type de réaction dans laquelle le catalyseur forme avec les réactifs (en l'occurrence, les gaz polluants) un système polyphasique. En effet, le catalyseur adsorbe, c'est-à-dire qu'il retient les molécules des réactifs à sa surface, affaiblissant leurs liaisons et accélérant le processus de réaction.
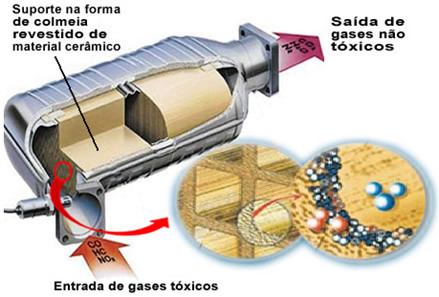
Ainsi, les métaux catalyseurs transforment des agents polluants tels que le CO et le NOX dans des gaz non toxiques comme le CO2, H2oh, oh2 et non2. Voir certaines de ces réactions ci-dessous et noter qu'à travers elles, il y a oxydation des hydrocarbures et CO (dérivé d'une combustion incomplète) et aussi la réduction des oxydes d'azote en azote gazeux (N2):
2 CO(g) + 2 NON(g) → 2 CO2(g) + 1 N2(g)
2 CO(g) + 1 O2(g) → 2 CO2(g)
2C2H6(g) + 7O2(g) →4 CO2(g) + 6H2O(v)
2 NON2(g) +4 CO(g) →1 N2(g) + 4 CO2(g)
2 NON2(g) →1 N2(g) + 2O2(g)
2 NON(g) →1 N2(g) + 1 O2(g)
Par Jennifer Fogaça
Diplômé en Chimie
La source: École du Brésil - https://brasilescola.uol.com.br/quimica/conversor-catalitico.htm
