Considérons l'équilibre chimique suivant à température constante :
3 heures2(g) + N2(g) 2 NH3(g)
Selon Gay-Lussac, la proportion de volumes de gaz participants à une réaction est égale au rapport des coefficients stoechiométriques respectifs. En termes simples, nous pouvons dire que le nombre de molécules présentes dans les réactifs et les produits est égal aux coefficients de l'équation.
Dans le cas ci-dessus, dans les réactifs nous avons 4 molécules et dans les produits nous avons 2 molécules, ce qui signifie que le volume des réactifs est plus grand et le volume des produits, plus petit.
Si nous augmentons la pression dans ce système, la balance se déplacera vers le plus petit volume pour diminuer cette pression. Dans le cas de la réaction que nous considérons, le déplacement se fera dans le sens direct de la formation du produit (NH3(g)).
Cependant, si l'on baisse la pression, la réaction se déplacera vers le plus grand volume, qui est le sens inverse, de formation de réactifs (3 H2(g) + N2(g)).
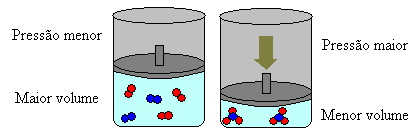
Cela se produit selon le principe de Le Chatelier, qui dit que toute perturbation (telle que la diminution ou l'augmentation de la pression) a causé dans un système en équilibre le fera se déplacer dans la direction qui minimise cette perturbation, se réajustant à un nouveau équilibre.
Brièvement, on peut dire ce qui suit dans le cas de l'influence de la variation de pression sur l'équilibre chimique :
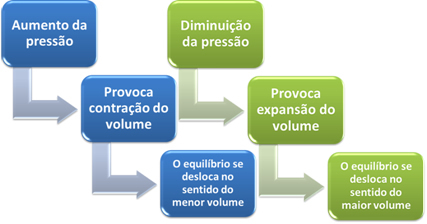
Dans le cas de réactions dans lesquelles le volume des réactifs est égal au volume des produits, l'équilibre chimique ne change pas.
Par Jennifer Fogaça
Diplômé en Chimie
La source: École du Brésil - https://brasilescola.uol.com.br/quimica/variacao-pressao-deslocamento-equilibrio-quimico.htm
