O neptunium, de symbole Np et de numéro atomique 93, est un métal appartenant à la série des actinides. C'est un métal de couleur grise, mais d'origine synthétique. Sur les 22 isotopes existants de Np, tous ont une demi-vie inférieure à la durée de vie de Np. planète, et, par conséquent, il n'est plus possible de trouver des quantités appréciables de cet élément dans les sources naturel.
En 1940, le neptunium était le premier actinide synthétisé, au moyen de techniques d'irradiation neutronique dans les isotopes de l'uranium. Bien qu'il n'y ait pas d'applications commerciales pour cet élément, le neptunium peut être utilisé dans la fabrication d'isotopes du plutonium, qui ont des applications nucléaires spécifiques.
A lire aussi: Tableau périodique complet et mis à jour
résumé sur le neptunium
Neptunium, symbole Np, c'est un métal appartenant au groupe des actinides.
Sous sa forme métallique, il présente une couleur grise.
Il est réactif avec l'air et les acides dilués. Il existe déjà plusieurs composés de neptunium connus.
Il existe 22 isotopes connus du neptunium, la masse 237 ayant la demi-vie la plus longue.
Il n'est pas possible de trouver du neptunium en quantité appréciable dans la nature, c'est donc un élément synthétique.
La principale forme de production est l'irradiation neutronique des isotopes de l'uranium.
Il n'y a pas d'utilisation commerciale du neptunium.
Il a été découvert en 1940 par McMillan et Abelson.
propriétés du neptunium
Symbole: Non.
numéro atomique: 93.
masse atomique: 237 a.u.m.a.
électronégativité: 1,36.
Point de fusion: 644 °C.
Point d'ébullition: 3902 °C.
Densité: 20.25 g.cm-3 (20°C).
configuration électronique: [Rn] 7s2 5f4 6d1.
série chimique: métaux, groupe 3, actinides, éléments de transition internes.
caractéristiques du neptunium
Le neptunium, symbole Np, est un métal appartenant à la série des actinides, située dans la septième période, groupe 3, du tableau périodique. Sous sa forme métallique, le neptunium présente une coloration argentée et forme une fine couche d'oxyde lorsqu'il est exposé à l'air à température ambiante. À des températures plus élevées, la réaction de formation d'oxyde est plus prononcée. Dans les aspects de la manipulation, le neptunium métallique ressemble uranium.
En solution aqueuse, le neptunium admet des indices d'oxydation compris entre +3 et +7. Il réagit avec les acides dilués et dégage de l'hydrogène gazeux., H2, mais n'est pas attaqué par des bases. Forme des tri et tétrahalogénures, tels que NpF3, NpF4, NpCl4, NpBr3 et NpI3, ainsi que des oxydes de différentes compositions, tels que Np3O8 et NpO2.
Vingt-deux isotopes de Np sont connus, le 237Np un isotope avec une demi-vie suffisante (2,144 x 106 années) à manipuler en quantités mesurables.
Où trouver le neptunium ?
Neptunium a été le premier élément transuranien à synthétiser, c'est-à-dire qu'il était produit en laboratoire. Penser que la planète Terre est d'environ 4,5 x 109 ans, pas même l'isotope à vie la plus longue de Np, celui de masse 237, ne parviendrait à être présent en quantité détectable.
Même ainsi, des traces de Np peuvent être détectées par des processus de désintégration d'atomes d'uranium présents dans des échantillons de minéraux. Cependant, on estime que la quantité de Np présente est un quadrillionième de la quantité d'uranium dans le minerai.
Obtention de Neptunium
Les principaux isotopes du neptunium sont produits par irradiation neutronique à l'uranium. Sur les 22 isotopes connus, seuls trois ont des demi-vies suffisamment longues pour s'accumuler: ceux de masse 235, 236 et 237. La synthèse de 237Np est le suivant.
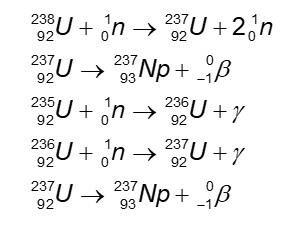
Les isotopes 238 et 239 sont également produits avec le 237Np, cependant, a une demi-vie très courte et ne s'accumule pas. Les isotopes 235 et 236 sont synthétisés par irradiation de 235U sur le cyclotron.
A lire aussi: Actinium - un autre métal rare et difficile à obtenir
applications du neptunium
Il n'y a pas d'utilisations commerciales pour le neptunium. Cependant, le 237Np est utilisé pour la synthèse de 238Pu (plutonium-238). Le plutonium, à son tour, est utilisé comme source de chaleur pour les générateurs thermoélectriques à radio-isotopes et les unités de chauffage à radio-isotopes. Le premier est utilisé pour fournir de l'électricité aux véhicules spatiaux des missions de la NASA telles que Galileo, Cassini et Ulysse. Le second est utilisé pour fournir de la chaleur aux instruments délicats des missions spatiales.
Le neptunium métallique peut être obtenu en réduisant NpF3 avec des vapeurs de baryum ou de lithium à une température d'environ 1200 °C.
histoire du neptunium
Neptunium était le premier actinide synthétisé en laboratoire. En 1940, McMillan et Abelson ont bombardé une fine couche d'oxyde d'uranium VI (UO3) avec des neutrons dans un cyclotron. Les résultats indiquent la création de deux nouveaux composants radioactifs: l'un avec temps de demi-vie de 23 minutes (identifié plus tard comme 239U) et un autre avec une demi-vie de 2,3 jours.
Après une enquête approfondie des résultats, il a été conclu que l'autre composant, avec une demi-vie plus longue, était l'élément de numéro atomique 93, avec une masse égale à 239.
Le nouvel élément s'appelait neptunium (l'orthographe «netunium» est également acceptée) en référence à la planète Neptune, qui est la première planète du système solaire après Uranus, car le nouvel élément viendrait juste après l'uranium. Cette façon de nommer un nouvel élément a également servi de paramètre pour l'élément 94, le plutonium, puisque la planète Pluton (jusqu'alors) orbite autour de Neptune.
Par Stefano Araujo Novais
Professeur de chimie

