Les colloïdes, solutions colloïdales ou système colloïdal sont des mélanges qui présentent l'aspect d'une solution, c'est-à-dire un mélange homogène. Mais en réalité ce sont des mélanges hétérogènes.
En effet, bien que cela ne soit pas clair à l'œil nu, la différence dans les mélanges colloïdaux peut être observée grâce à l'utilisation d'instruments tels que le microscope.
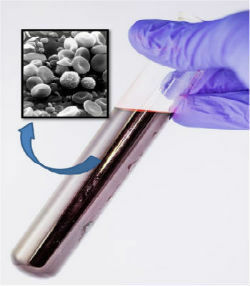 Le sang, bien qu'apparaissant homogène, à l'aide d'un microscope, nous avons observé qu'il est composé de plusieurs composants.
Le sang, bien qu'apparaissant homogène, à l'aide d'un microscope, nous avons observé qu'il est composé de plusieurs composants.
Les colloïdes sont présents dans notre vie quotidienne. Elles sont exemples de colloïdes: crème hydratante, yaourt, lait, sang, colorants et confiture.
C'est pour cette raison que certains produits chimiques indiquent qu'ils doivent être secoués avant d'être utilisés. Cela doit être fait pour unir les particules colloïdales.
Dans le même temps, les mélanges colloïdaux ne se déposent pas naturellement. Si on met un colloïde dans un récipient, les particules ne se déposent pas au fond. Ils ne peuvent pas non plus être filtrés.
La taille des particules présentes dans les colloïdes est comprise entre 1 et 100 nanomètres (1 nanomètre équivaut à 1 millionième de millimètre).
Tout ce qui se trouve en dehors de cette plage est mélanges homogènes ou hétérogènes.
Les mélanges homogènes sont considérés comme de vraies solutions. Ses particules sont inférieures à 1 nanomètre. Les mélanges hétérogènes ont des particules de plus de 100 nanomètres.
En savoir plus sur Solutions chimiques et Séparation des mélanges.
Quelles sont vos propriétés ?
Les composants des colloïdes sont appelés éparpillé et dispersant. La quantité de dispersant est toujours plus élevée.
Apparemment, ils assument une caractéristique de mélange homogène.
Les blancs d'œufs battus sur neige en sont un exemple: le blanc sous forme liquide joue le rôle de composant dispersé.
L'air, qui a transformé le blanc en mousse, est le composant dispersant, car il a fallu plus d'air que le blanc pour réaliser ce mélange.
De plus, les colloïdes laissent passer la lumière entre eux, ce qui n'est pas le cas des mélanges homogènes.
Si l'on dirige une lampe torche avec un petit faisceau lumineux vers un mélange colloïdal, il est possible de voir un faisceau lumineux traverser tout le récipient où il se trouve. C'est comme ça que ça s'appelle Effet Tyndall.
Grâce à la même expérience, il est également possible de détecter le mouvement aléatoire des particules dans le mélange. C'est appelé mouvement brownien.
Bref, le propriétés des systèmes colloïdaux elles sont:
- Les phases du mélange ne sont pas facilement distinguables ;
- La gamme de tailles de particules est de 1 et 100 nanomètres;
- effet Tyndall ;
- Présence de particules dispersées et de dispersants ;
- Ils ne se déposent pas naturellement et ne peuvent pas non plus être filtrés ;
- Mouvement brownien.
Types de colloïdes
Les colloïdes sont classés selon l'état physique des particules dispersées et dispersantes.
Les types de colloïdes sont: aérosol, émulsion, mousse, gel et sol (ceux qui ressemblent à une solution). En savoir plus sur chacun d'eux :
Aérosol
Composant dispersé: Solide ou Liquide
Composant dispersant: gaz
Exemples: Fumée, brouillard, nuage, embruns
Émulsion
Composant dispersé: Liquide
Composant dispersant: Liquide ou Solide
Exemples: Mayonnaise, beurre, fromage, glace
Mousse
Composant dispersé: gaz
Composant dispersant: Liquide ou Solide
Exemples: Crème fouettée, blanc en neige, mousse à raser, pop corn
Gel
Composant dispersé: Liquide
Composant dispersant: solide
Exemples: Gélatine, gel de silice, dentifrice
Soleil
Composant dispersé: solide
Composant dispersant: Liquide ou Solide
Exemples:Perle, Rubis, Sang
Pour en savoir plus, découvrez une méthode de séparation des mélanges colloïdaux, le Centrifugation.



