Amines sont des composés organiques azotés dérivés de la substance ammoniac (NH3) en remplaçant un ou plusieurs hydrogènes par des radicaux organiques. Selon la quantité d'hydrogènes substitués, le amines peut être classé en :
Amine primaire : formé en remplaçant un hydrogène dans l'ammoniac par un radical organique;
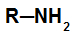
Structure générale d'une amine primaire
Amine secondaire : formé par le remplacement de deux hydrogènes d'ammoniac par deux radicaux organiques.

Structure générale d'une amine secondaire
Amine tertiaire : formé en remplaçant les trois hydrogènes de l'ammoniac par trois radicaux organiques.

Structure générale d'une amine tertiaire
Caractéristiques physiques des amines
Ce sont des composés polaires ;
Les amines primaires et secondaires sont capables d'effectuer liaisons hydrogène;
Les amines tertiaires effectuent une interaction dipôle permanent;
Les amines contenant jusqu'à cinq atomes de carbone sont solubles dans l'eau et l'éthanol. Les amines avec six carbones ou plus sont pratiquement insolubles dans l'eau, mais solubles dans les solvants organiques ;
Les amines qui ont une structure aromatique sont plus denses que l'eau ;
Les amines avec un à trois carbones sont gazeuses à température ambiante. Ceux avec quatre à douze carbones sont liquides à température ambiante ;
En général, les amines ont des points de fusion et d'ébullition plus élevés que par rapport à tout composé organique non polaire.
Caractéristiques chimiques des amines
Ils sont considérés comme des bases organiques, selon la théorie de Bronsted-Lowry ;
Les amines aromatiques ont un caractère basique plus faible en raison du phénomène de résonance;
Plus le caractère basique de l'amine est grand, plus elle est susceptible de réagir avec une certaine substance ;
En présence d'un acide, les amines effectuent réaction de neutralisation, car ils ont un caractère de base.
Règle de nomenclature des amines
Pour nommer une amine, il suffit de suivre la règle établie par l'Union internationale de chimie pure et appliquée (IUPAC), décrite ci-dessous :
Nom du ou des radicaux + amine
REMARQUE: Si l'amine a des radicaux différents, il faut suivre l'ordre alphabétique.
Suivez quelques exemples :
Exemple 1: amine primaire

Dans l'amine primaire de cet exemple, nous avons la présence d'un radical propyle, son nom est donc propylamine.
Exemple 2 : amine secondaire

Dans l'amine secondaire de cet exemple, on a la présence du radical méthyle (à gauche de l'azote) et du radical éthyle (à droite de l'azote). Son nom est, par ordre alphabétique, éthyl-méthylamine.
Exemple 3 : amine tertiaire
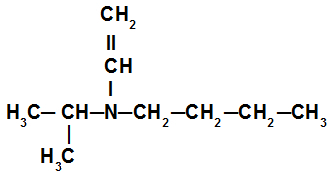
Dans l'amine secondaire dans cet exemple, nous avons le radical isopropyle (à gauche de l'azote), le radical butyle (à droite de l'azote) et le radical vinyle (en dessous de l'azote). Son nom est donc butyl-isopropyl-vinylamine.
Applications d'amines
Largement utilisé dans la production de divers composés organiques;
Utilisé dans la fabrication de savons;
Utilisé dans le processus de vulcanisation du caoutchouc;
Utilisé dans la fabrication de colorants.
Par moi Diogo Lopes Dias
La source: École du Brésil - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-sao-aminas.htm


