Les fonctions d'azote sont l'un des 4 groupes fonctionnels des composés organiques. Les composés qui appartiennent à cette fonction sont formés par l'azote, ils sont donc appelés composés azotés. Les principaux sont les amines, les amides, les nitriles et les composés nitro.
Amines
À amines sont des composés organiques qui peuvent être trouvés à l'état solide, liquide ou gazeux. Ils sont produits par la décomposition des animaux et peuvent également être trouvés dans des composés extraits de plantes.
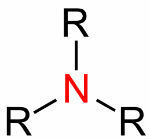
Formule générale des amines
Ils sont dérivés d'aryle ou d'alkyle en relation avec l'azote. Aryle et alkyle remplacent les atomes d'hydrogène. Selon ce remplacement, ils peuvent être classés comme suit :
- Primaire: lorsqu'un seul hydrogène est remplacé (R-NH2). Exemple: la méthanamine.
- Secondaire: lorsque deux hydrogènes sont remplacés (R1R2NH). Exemple: diméthaneamine.
- Tertiaire: lorsque trois hydrogènes sont remplacés (R1R2R3N). Exemple: triéthaneamine.
Les amines sont utilisées dans la fabrication de colorants, de médicaments et de savons.
La nomenclature des amines est formée comme suit :
- remplacer le suffixe d'hydrocarbure « o » par le mot amine.
- indiquant la position de l'azote.
- indiquant le type de reliure an, en ou in.
amides
À amides sont des composés organiques qui peuvent être trouvés à l'état solide ou liquide. Ils sont dérivés d'un acyle lié à l'azote et produits en laboratoire.
La formule moléculaire des amides est CONH2, qui est représenté comme suit :
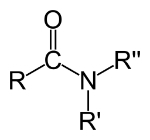
Formule générale des amides
Les amides sont classés selon le nombre d'acyles liés à l'azote qui ont :
- Primaire: lorsqu'il ne possède qu'un seul groupe acyle R-CO)NH2.
- Secondaire: lorsqu'ils possèdent deux groupes acyle (R-CO)2NH.
- Tertiaire: lorsqu'ils possèdent trois groupements acyle (R-CO)3N.
Quant au nombre de groupements amides présents, la classification est la suivante :
Les diamides, lorsqu'il y a deux groupes d'amides, et les triamides, lorsqu'il y a trois groupes d'amides, etc.
Ses applications dans la vie quotidienne: fabrication de produits cosmétiques de soins personnels (gel douche) et de produits de nettoyage (détergents), entre autres.
Le nom des amides est formé par le préfixe, qui indique le nombre de carbones. Ensuite, le suffixe « oico » pour hydrocarbure est remplacé par le mot amide.
Composés nitro
Les composés nitro sont des composés organiques présents à l'état liquide qui ne se dissolvent pas dans l'eau car ils sont denses et très réactifs. La formule générale des composés nitro est AU2.
L'application des composés nitro est complète. Ils sont utilisés comme explosif, comme solvant et également dans la fabrication de pommades et d'outils.
Le nom des composés nitro est formé en joignant le nom de la chaîne principale avec le mot nitro.
Nitriles
Les nitriles, également appelés cyanures, sont des composés organiques présents à l'état solide et solubles dans l'eau. La formule générale des nitriles est R — C N.
Ces composés sont utilisés dans la fabrication de caoutchouc, de colorants, d'engrais et de plastiques.
Le nom des nitriles est formé en joignant le nom de l'hydrocarbure avec le mot nitrile.
Lire aussi Fonctions oxygénées.
Des exercices
1. (Cesgranrio-RJ) Au début de 1993, les journaux rapportaient que lorsqu'une personne tombe amoureuse, la organisme synthétise une substance - l'éthylphénylamine, responsable de l'excitation caractéristique de cette Etat.
La classification et le caractère chimique de cette amine sont respectivement :
a) amine primaire – acide.
b) amine primaire – basique.
c) amine secondaire – neutre.
d) amine secondaire – acide.
e) amine secondaire – basique.
Alternative e: amine secondaire – basique.
2. (UnB-DF) L'acétoaminophène est une substance qui possède des propriétés analgésiques et antipyrétiques. Il est commercialisé sous le nom de Tylenol et sa formule est décrite ci-dessous :
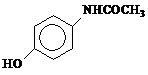
Cochez les bonnes alternatives concernant l'acétoaminophène.
1. Il appartient à la classe des phénols ;
2. Il contient également la fonction amide ;
3. A la formule C8H9AU2;
4. Il appartient à la classe des substances aromatiques en raison de la présence du cycle benzénique.
Toutes les alternatives sont correctes