L'ébullition est le passage d'un état liquide à un état gazeux. Cela se produit lorsqu'une portion de liquide, soumise à une pression donnée, reçoit de la chaleur et atteint une certaine température.
La quantité de chaleur que le corps doit recevoir pour se transformer complètement en vapeur dépend de la substance qui le constitue.
Une substance à l'état liquide n'a pas de forme définie, prenant la forme du récipient qui la contient.
Étant pratiquement incompréhensible, il présente une force de cohésion entre les particules qui le constituent.
Pour passer à l'état gazeux, la substance doit recevoir de la chaleur. Cette augmentation d'énergie fera vibrer les molécules avec une plus grande intensité, augmentant la distance entre elles.
De cette façon, la force de cohésion devient pratiquement inexistante. Le corps dans cet état n'a pas de forme ou de volume défini.
Les geysers sont des exemples d'ébullition qui se produit avec les eaux souterraines situées dans les régions volcaniques. Le magma chauffe l'eau et lorsqu'elle atteint une certaine température, elle commence à changer d'état.
La vapeur occupe un volume plus important, augmentant la pression dans la cavité souterraine. En conséquence, un mélange de vapeur et de liquide est expulsé vers la surface par de petites fissures.

Caractéristiques d'ébullition
Un liquide bout selon le schéma suivant :
- En maintenant la pression constante, la température tout au long du processus d'ébullition restera constante.
- La quantité de chaleur par unité de masse nécessaire pour qu'un liquide se transforme complètement en vapeur est appelée chaleur latente de vaporisation. Sa valeur dépend de la substance qui compose le liquide.
- La température à laquelle chaque substance bout est bien déterminée et s'appelle le point d'ébullition.
Conseil: Lors de la cuisson des aliments, c'est une bonne idée de baisser le feu lorsque l'eau commence à bouillir. Comme la température reste constante tout au long du processus d'ébullition, le temps de cuisson sera le même à feu vif ou feu doux. De cette façon, nous économisons du gaz et l'environnement nous en est reconnaissant.
Quantité de chaleur latente
La quantité de chaleur qu'un liquide doit recevoir pour se transformer en vapeur dépend de la valeur de la chaleur latente de vaporisation et de sa masse.
Ci-dessous, nous présentons la valeur de la chaleur latente de vaporisation de certaines substances :

Formule
Pour calculer la quantité de chaleur nécessaire pour qu'un liquide change d'état, nous utilisons la formule suivante :
Où,
Qv: quantité de chaleur (chaux)
m: masse (g)
Lv: chaleur latente de vaporisation (cal/g)
Exemple:
Quelle quantité de chaleur faut-il pour que 100 g d'éthanol bouillent et se transforment complètement en vapeur ?
Qv = 100. 204 = 204 000 cal
Température d'ébullition
La température à laquelle un corps subit une ébullition dépend de la substance qui le compose et de la pression à laquelle il est soumis.
Le point d'ébullition des substances est déterminé en laboratoire. Par exemple, le point d'ébullition de l'eau, soumise à 1 atmosphère, est de 100°C. Le fer est à 2800 °C, tandis que l'hydrogène est à - 252,8 °C.
Pour connaître la température de changement de phase d'autres substances, lisez aussi point d'ébullition.
Moins un corps est soumis à une pression, plus son point d'ébullition est bas. Cela signifie que dans les villes à haute altitude, la cuisson des aliments prend beaucoup plus de temps.
Pour cuire les aliments plus rapidement, nous utilisons des autocuiseurs. Ce type de cuisinière utilise un système d'étanchéité qui rend la pression à l'intérieur supérieure à la pression atmosphérique.
La pression plus élevée augmente également le point d'ébullition. Dans le cas de l'eau, elle bouillira à une température pouvant atteindre 120 ºC, réduisant ainsi le temps de cuisson.
changements de phase
Le passage d'un état liquide à un état gazeux est appelé génériquement vaporisation, car il englobe, en plus de l'ébullition, deux autres procédés: évaporation et chauffage.
L'évaporation se produit progressivement, n'ayant pas besoin d'atteindre une température spécifique pour se produire. D'autre part, le chauffage se produit lorsque nous plaçons le liquide sur une surface dont la température est supérieure à son point d'ébullition.
Il existe encore d'autres processus de changement d'état. Sont-ils:
- La fusion
- Solidification
- Liquéfaction ou condensation
- Sublimation
Dans le schéma ci-dessous, nous représentons les trois états physiques de la matière et les changements d'état respectifs :
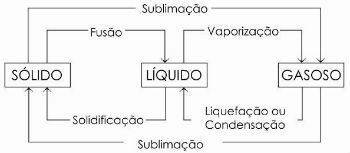
Pour en savoir plus, lisez aussi États physiques de l'eau.
Des exercices
Enem - 1999
Le texte doit être utilisé pour les deux questions suivantes.
L'autocuiseur permet de cuire les aliments dans l'eau beaucoup plus rapidement que les autocuiseurs conventionnels. Son couvercle est muni d'un joint en caoutchouc qui ne laisse pas s'échapper la vapeur, sauf par un trou central sur lequel repose un poids qui contrôle la pression. Lors de l'utilisation, une haute pression s'accumule à l'intérieur. Pour son fonctionnement en toute sécurité, il est nécessaire de respecter la propreté du trou central et l'existence d'une soupape de sécurité, normalement située dans le couvercle.
Le schéma de l'autocuiseur et un diagramme des phases de l'eau sont présentés ci-dessous.
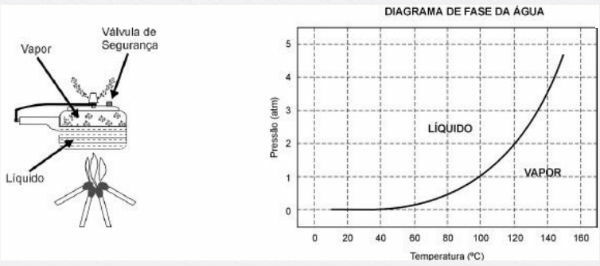
1) L'avantage d'utiliser un autocuiseur est la vitesse de cuisson des aliments et cela est dû à
a) la pression à l'intérieur, qui est égale à la pression à l'extérieur.
b) la température de son intérieur, qui est supérieure à la température d'ébullition de l'eau du lieu.
c) la quantité de chaleur supplémentaire qui est transférée à la casserole.
d) la quantité de vapeur libérée par la vanne.
e) l'épaisseur de sa paroi, qui est supérieure à celle des casseroles courantes.
Alternative b: à sa température intérieure, qui est supérieure à la température d'ébullition de l'eau du lieu.
2) Si, par économie, on baisse le feu sous cocotte minute dès que la vapeur sort par la vanne, afin de simplement garder le temps d'ébullition, le temps de cuisson
a) il sera plus gros car la casserole « refroidit ».
b) sera plus petit, car il réduit la perte d'eau.
c) sera d'autant plus grande que la pression diminue.
d) sera d'autant plus grande que l'évaporation diminuera.
e) ne changera pas car la température ne change pas.
Alternative e: ne sera pas modifiée car la température ne varie pas.


