LES constante d'ionisation donne L'eau(Kw), O potentiel d'hydrogène(pH) C'est le potentiel hydroxylionique (pOH) elles sont les mesures important pour les calculs impliquant équilibre chimique dans des solutions acides et basiques, ainsi que dans la détermination de la concentration en ions H+ et oh- des solutions en question.
Qu'est-ce que Kw?
Le produit ionique de l'eau, ou Kw (ce wmoyens l'eau — water, en anglais), est la constante utilisée pour représenter la équilibre généré par l'auto-ionisation de l'eau. Même à un très faible taux, l'eau s'ionise en produisant des ions H+ et oh-, selon l'équation chimique suivante :
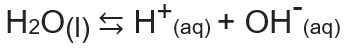
En analysant l'équation, on se rend compte que lorsque le ionisation à partir d'une molécule d'eau pure, un ion H est généré.+ et un ion OH-, C'est le la concentration de ces ions sera toujours la même. Même lorsqu'il y a une augmentation de la température, ce qui provoque une augmentation du taux d'ionisation, les concentrations restent les mêmes.
A lire aussi :Énergie d'ionisation
Ne vous arrêtez pas maintenant... Y'a plus après la pub ;)
Sur la base de mesures expérimentales, la concentration en ions H a été calculée+ et oh- (résultant de l'auto-ionisation de l'eau) à 25°C et la valeur de 1. 10-7 mol/L. C'est-à-dire, d'un total de 1 milliard de molécules d'eau, seul deux subissent une ionisation. Cela montre que l'eau pure a un faible degré d'ionisation et explique la très faible Conductivité électrique d'eau pure.
Compte tenu de ce qui a été montré ci-dessus, nous pouvons écrire le expression de la constante de bilan hydrique :

Utilisation des valeurs de concentration en ions H+ et oh- à 25°C, on peut calculer la valeur de Kw :
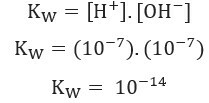
Comme indiqué précédemment, cette valeur de Kw change avec l'augmentation de la température, comme indiqué dans le tableau ci-dessous :
T (°C) |
Kw |
10 |
0,29. 10-14 |
20 |
0,68. 10-14 |
25 |
1,00. 10-14 |
30 |
1,47. 10-14 |
40 |
2,92. 10-14 |
60 |
9,40. 10-14 |
Pour en savoir plus sur ce sujet, lisez notre texte: Produit d'eau ionique.
Qu'est-ce que le pH et le pOH ?

l'acronyme pH moyens potentiel d'hydrogène et a été créé par le biochimiste danois Soren Sorensen, en 1909, pour faciliter le travail avec le concentrations en ions hydrogène [H+], qui sont généralement exprimés en nombres décimaux. Pour en savoir plus sur ce sujet, lisez notre texte: Qu'est-ce que le pH ?
Ce genre de notation indique la teneur en ions H+ présent dans la solution et est défini par l'expression mathématique :
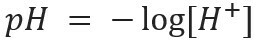
De même, on peut définir le pOH ou potentiel hydroxylionique, qui nous indique le Teneur en ions OH- présent dans la solution. Son expression mathématique est :
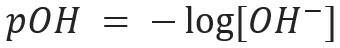
Dans une solution aqueuse, il y aura toujours des ions H+ et oh- (due à l'ionisation subie par l'eau) qui servira à caractériser une solution en acide ou alors de base. Plus il y a d'ions H+ il y a dans la solution, plus elle sera acide. Par conséquent, la présence d'ions OH- dans la solution le rendra plus basique. S'il y a un équilibre dans la quantité de ces ions, la solution sera classée comme neutre.
échelle de pH
L'échelle de pH est affichée avec des valeurs allant de 0 à 14 (valeurs mesurées à 25°C). Voir l'échelle de pH dans l'image ci-dessous :

Plus le pH est basde la solution,plus grande est son acidité, et plus on se rapproche de la fin de l'échelle, c'est-à-dire plus près de 14, plus son caractère fondamental est grand. Par exemple, le jus de citron a un pH de 2, tandis que les agents de blanchiment ont un pH de 12.
Comment calculer le pH et le pOH
connaissant le concentration en ions, nous pouvons calculer les valeurs du pH et du pOH des solutions, et, connaissant les valeurs potentielles, on calcule le concentration d'ions dans les solutions. A cet effet, les expressions suivantes sont utilisées :
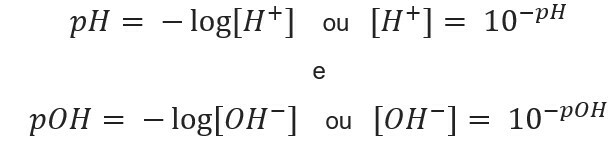
Passons aux exemples :
Exemple 1
Si on veut connaître le pH d'une solution avec [H+] = 0,001 mol/L, il suffit d'utiliser la formule présentée précédemment :
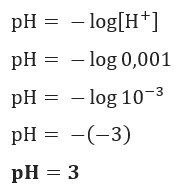
Exemple 2
Maintenant, pour savoir quelle est la concentration de OH- d'une solution avec pOH = 5, remplacez simplement la valeur dans la formule suivante :

Si on applique la même échelle de potentiel pour le bilan ionique de l'eau, on aura :
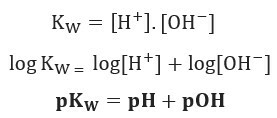
Comme indiqué, à 25°C, Kw = 10-14. Par conséquent:

Avec cela, nous pouvons calculer le pOH d'une solution en fonction de son pH. Si nous avons une solution avec un pH de 3, alors son pOH sera de 11.
Savoir plus: Milieux neutres, acides et basiques
Exercices résolus
Question 1 (UEFS-BA) La concentration des ions OH–(ici) dans une solution d'hydroxyde d'ammonium donnée, à 25 °C, est égal à 1,10–3 mol/L. Le pOH de cette solution est :
a) 0
b) 1
c) 3
d) 11
e) 13
Résolution: Lettre C. Si nous avons [OH–] = 10–3 mol/L, donc votre pOH sera égal à 3.
Voir:
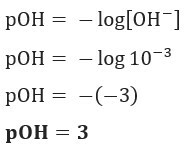
Question 2 (UEA-AM) Considérez les informations suivantes, obtenues à partir d'un label d'eau minérale dans la ville de Porto Seguro (BA):
nitrate 1,45 mg/L
pH à 25°C 4,51
Cette eau minérale est
a) acide et a [H+] < [OH–].
b) acide et a [H+] > [OH–].
c) neutre et a [H+] = [OH–].
d) basique et a [H+] > [OH–].
e) basique et a [H+] < [OH–].
Résolution: La lettre B. Comme le pH de l'eau minérale indiqué sur l'étiquette est inférieur à 7, on peut dire qu'il s'agit d'une solution acide et, par conséquent, la concentration en ions H+ est plus grand que les OH-.
Question 3 (UEA-AM) Une façon de produire rapidement de l'hydrogène gazeux en laboratoire consiste à faire réagir du zinc métallique en poudre avec de l'acide chlorhydrique (HCl), à une concentration de 1,0 mol/L :
Zn (s) + 2 HCl (aq) → ZnCl2 (aq) + H2 (g)
Considérant que l'acide chlorhydrique est ionisé à 100 % et que la solution est à 25°C, il est correct d'affirmer que le pH de la solution d'acide chlorhydrique mentionné dans le texte est
- 0
- 1
- 3
- 13
- 14
Résolution:Lettre a. On peut calculer le pH de la solution à partir de la concentration en HCl renseignée dans le texte, puisque, comme il est ionisé à 100 %, la concentration en [H+] sera le même, car pour chaque molécule de HCl ionisée, un ion H+ sera généré. Par conséquent:
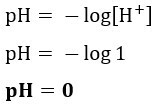
Par Victor Ferreira
Professeur de chimie