ils s'appellent éléments de transition intérieurs tous les 28 éléments chimiques situé en 6e et 7e période du groupe 3 (ou famille IIIB) de la Tableau périodique. Ils sont positionnés plus spécifiquement à l'extérieur du corps principal de la Table.
sont appelés éléments de transition car ils n'appartiennent pas aux familles A (éléments représentatifs), mais ils ne peuvent être confondus avec les éléments de transition externe (éléments appartenant aux familles B et positionnés dans le corps principal du tableau Périodique).
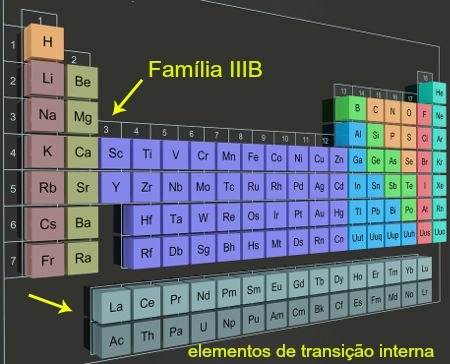
Éléments de transition internes dans les colonnes situées en dehors du tableau périodique
Toi éléments de transition intérieurs présenter le sous-niveau f comme plus énergétique. Une preuve en est que chacune des colonnes horizontales se référant à ces éléments n'a que 14 éléments, 14 étant le nombre maximum de électrons pris en charge par le sous-niveau f.
a) Série des lanthanides
Les lanthanides sont tous ceux qui appartiennent exclusivement à la 6ème période de la famille IIIB, ainsi nommés car le premier élément de la série est le lanthane (La). Voir les noms et acronymes de chacun d'eux :
Lanthane (La)
Cérium (C)
Praséodyme (Pr)
Néodyme (Nd)
Prométhium (Pm)
Samarium (Sm)
Europium (I)
Gadolinium (Gd)
Terbium (Tb)
Dysprosium (Dy)
Holmium (Ho)
Erbium (Euh)
Thulium (Tm)
Ytterbium (Yb)
Tous les éléments de transition internes présentent le sous-niveau 4f comme le plus énergétique, c'est-à-dire le diffusion électronique de tous se termine à ce sous-niveau, comme on peut le voir dans la distribution de deux éléments appartenant à la série :
Ne vous arrêtez pas maintenant... Y'a plus après la pub ;)
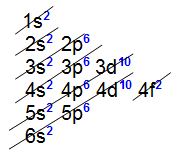
Distribution électronique de l'élément lanthanide Cerium

Distribution électronique de l'élément lanthanide Holmium
b) Série des actinides
Les actinides sont tous ceux qui appartiennent exclusivement à la 7ème période de la famille IIIB, ainsi nommés car le premier élément de la série est l'actinium (Ac). Voir les noms et acronymes de chacun d'eux :
Actinium (Ac)
Thorium (Th)
Protactinium (Pa)
Uranium (U)
Neptunium (Np)
Plutonium (Pu)
Américium (Am)
Curium (cm)
Berkélium (Bk)
Californie (Cf)
Einsteinium(s)
Fermium (Fm)
Mendelevium (Md)
Nobel (Nb)
Tous les éléments de transition internes présentent le sous-niveau 5f comme le plus énergétique, c'est-à-dire la distribution l'électronique de tous se termine à ce sous-niveau, comme on peut le voir dans la répartition de deux éléments appartenant à les séries:

Distribution électronique de l'élément actinide d'uranium

Distribution électronique de l'élément actinide de Californie
Par moi Diogo Lopes Dias
Souhaitez-vous référencer ce texte dans un travail scolaire ou académique? Voir:
JOURS, Diogo Lopes. « Éléments de transition internes »; École du Brésil. Disponible en: https://brasilescola.uol.com.br/quimica/elementos-transicao-interna.htm. Consulté le 27 juin 2021.