Métaux sont des éléments caractérisés par la luminosité, la résistance, la conductivité thermique et électrique. Elles sont applicable dans pratiquement tous les processus industriels, étant présent dans les alliages métalliques utilisés dans la fabrication d'outils, de bijoux et de pièces de monnaie et dans des procédés chimiques tels que le redox, responsable du fonctionnement de piles et piles.
Dans le tableau périodique, ils sont classés en :
semi-métaux
métaux de transition
métaux alcalins
métaux alcalino-terreux
Dans l'industrie sidérurgique, ils sont séparés en:
métaux ferreux
Métaux non-ferreux
métaux lourds
A lire aussi: Quels sont les nouveaux éléments du tableau périodique ?
Caractéristiques du métal

Ils sont, pour la plupart, d'excellents conducteurs de chaleur et d'énergie électrique.
Ils ont un aspect brillant.
avoir haut densité.
Ce sont des éléments électropositifs (ils ont tendance à former des cations — des charges positives).
A l'exception du Mercure, ce sont des éléments à haut point de fusion et solides à température ambiante.
Ils ont une résistance mécanique (ténacité).
Ils sont malléables (peuvent être moulés sans se casser).
Ne vous arrêtez pas maintenant... Y'a plus après la pub ;)
Tableau périodique des métaux
métaux alcalins
Les éléments de première colonne du tableau périodique, famille 1A. Ils sont appelés métaux alcalins car, lorsqu'ils sont mélangés à de l'eau, ils forment des hydroxydes, c'est-à-dire une solution alcaline (basique).
Toi éléments qui appartiennent à ce groupe sont :
Lithium (li)
Sodium (À)
Potassium (K)
Rubidium (Rb)
Césium (Cs)
Francio (Fr)
La configuration électronique des métaux alcalins à l'état neutre (non chargé/ionisé) ne présente que un électron dans la dernière couche (couche de valence). O rayon atomique et la réactivité de ces métaux augmente de haut en bas (en observant la Tableau périodique). Ils ont un point de fusion bas par rapport aux autres métaux, sont malléables et peu denses, ont un aspect mat dû à la potentiel d'oxydation élevé.
Voir aussi :Quelles sont les propriétés de la matière ?
métaux alcalino-terreux
Ce sont des éléments qui apparaissent dans le deuxième colonne du tableau périodique, famille 2A. sont appelés Terre alcaline par la tendance à former des solutions à caractère basique (alcalin), et par la terre car, avant le 19ème siècle, les oxydes formés par ces substances étaient désignés ainsi. Ce terme a été utilisé pour désigner les métaux non insolubles qui ne subissent pas de mutation lorsqu'ils sont chauffés, caractéristiques communes des éléments du groupe 2. Plus tard, à la lumière de nouvelles recherches et expériences, il a été découvert que les éléments «terrestres» étaient en fait des oxydes formés par des métaux.
Ce sont des métaux malléables, de faible densité, deux électrons dans sa couche la plus externe, se retrouvent, dans les conditions normales de température et de pression, à l'état solide. Appartenir à ce groupe :
Béryllium (Être)
Magnésium (mg)
Calcium (Ici)
Strontium (M.)
Baryum (Bah)
Radio (La grenouille)
métaux de transition
composent le groupe B du tableau périodique, et sont situés entre les métaux alcalino-terreux et le amétaux. Ils ont été définis par l'IUPAC comme des éléments qui ont une sous-couche énergétique energéticad’ incomplète. Le terme "métaux de transition" fait référence à passage du groupe 2 au 13 dans le tableau périodique et l'addition croissante d'électrons dans l'orbitale «d».
Le groupe des métaux de transition est composé d'éléments denses, avec des points de fusion et d'ébullition élevés, et moins réactif que les métaux des groupes 1 et 2 (Famille 1A et 2A). Parmi les métaux de transition figurent le tungstène, qui est l'élément ayant le point de fusion le plus élevé (3422 °C), et le mercure (Hg), qui est un métal liquide dans des conditions normales de température et de pression, son point de fusion est de (-38,83 °C).
Les métaux de transition ont divers états d'oxydation (NOX variable) et forment des substances colorées.

Éléments de transition internes
Éléments de transition internes elles sont:
Lanthanides : série composée d'éléments qui ont de 57 à 71 protons et qui, à l'exception du prométhium, sont naturels.
Actinides : groupe formé par les éléments allant de 89 à 103 en numéro atomique et qui, pour la plupart, sont synthétiques. Tout ce groupe est radioactif avec une demi-vie courte.
Les éléments de ces deux groupes ont un point de fusion élevé et sont tous solides à température ambiante.
Semi-métaux
Toi semi-métaux il y a, en tout, sept éléments :
Bore (B)
Silicium (Si)
Germanium (Ge)
Arsenic (As)
Antimoine (Lun)
Tellure (Te)
Polonium (Po)
Cette classification est donnée aux éléments qui ont caractéristiques physico-chimiques pertinentes pour les métaux et aussi d'autres pour les éléments non métalliques. Les semi-métaux ont un brillant, sont des composés cassants, capables de former des cations et aussi des anions (selon l'état), et sont des conducteurs intermédiaires.
Types de métaux
Ferreux: substances qui contiennent du fer dans leur composition. Elles sont les alliages de métaux qui contiennent du fer comme élément commun, mais peuvent être formulés avec différentes concentrations de carbone, par exemple, ou forgés avec des techniques différentes, ayant ainsi des produits avec des propriétés physiques différentes.
Non ferreux : alliages formés par d'autres types de métaux, tels que aluminium, cuivre, nickel, zinc, titane.
Métaux lourds: plomb, nickel, zinc, mercure. Ce sont des métaux réactifs, toxiques et bioaccumulables. Ils sont utilisés dans les batteries, les lampes, les munitions pour les artefacts militaires, entre autres.
Liaisons chimiques des métaux
Les métaux sont éléments électropositif, c'est-à-dire qu'ils ont tendance à perdre des électrons dans une liaison chimique. Lorsqu'un métal interagit avec un non-métal, il effectuer une liaison ionique en raison de la différence de électronégativité. L'autre possibilité de liaison pour les métaux est les liaisons métalliques.
À connexions métalliques se produisent entre les métaux, avec libération partielle d'électrons et formation d'un nuage ou d'une mer d'électrons autour des atomes, ce qui garantit aux pièces métalliques les propriétés de conductivité électrique et malléabilité.
Voir aussi: Conducteurs et isolants – quelles sont les différences ?
Obtention de métaux
La plupart des métaux se trouvent naturellement dans roches et minéraux associés à d'autres éléments. Il existe plusieurs techniques pour raffiner les métaux, telles que l'électrolyse et les réactions chimiques pour séparer les composés.
Dans le cas des métaux, les deux techniques les plus utilisées à l'échelle industrielle pour obtenir un certain degré de pureté dans un métal sont: différence de densité et susceptibilité magnétique (tendance que le métal doit réagir à un champ magnétique).

Exercices résolus
Question 1 - (Enem) Le cadmium, présent dans les batteries, peut atteindre le sol lorsque ces matériaux sont rejetés de manière irrégulière dans l'environnement ou lorsqu'ils sont incinérés. Contrairement à la forme métallique, les ions Cd2+ sont extrêmement dangereux pour l'organisme car ils peuvent remplacer les ions Ca2+, provoquant une maladie dégénérative des os, les rendant très poreux et provoquant une douleur intense dans les os. les articulations. Ils peuvent également inhiber les enzymes activées par le cation Zn2+, qui sont extrêmement importantes pour le fonctionnement des reins. La figure montre la variation du rayon de certains métaux et de leurs cations respectifs.
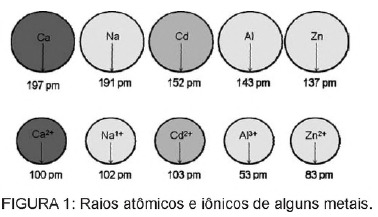
D'après le texte, la toxicité du cadmium sous sa forme ionique est une conséquence de cet élément
A) présentent une faible énergie d'ionisation, ce qui favorise la formation de l'ion et facilite sa liaison à d'autres composés.
B) ont tendance à agir dans des processus biologiques médiés par des cations métalliques avec des charges allant de +1 à +3.
C) ont un rayon et une charge relativement proches des ions métalliques qui agissent sur les processus biologiques, provoquant des interférences dans ces processus.
D) ont un grand rayon ionique, ce qui lui permet d'interférer dans les processus biologiques auxquels participent normalement des ions plus petits.
E) ont une charge +2, ce qui lui permet d'interférer avec les processus biologiques auxquels participent normalement des ions de charges plus faibles.
Résolution
Variante C. Le cadmium est un élément similaire aux ions métalliques que nous avons naturellement dans le corps. En plus d'être bioaccumulable, le cadmium, ayant cette similitude avec les groupes métalliques, peut se lier aux groupes sulfhydryle des molécules de protéines, provoquant ainsi des changements dans les processus biologiques, tels que la décalcification et la destruction des tissus et des globules rouges du sang.
Question 2 - Pour les caractéristiques relatives aux métaux, cochez la mauvaise alternative.
A) La plupart des métaux sont de bons conducteurs électriques et thermiques.
B) Certains métaux sont sensibles à l'oxydation et/ou à la réduction.
C) Le fer est un métal résistant et malléable, c'est-à-dire qu'il est facile à mouler.
D) Les métaux alcalino-terreux portent ce nom « terre » en référence aux oxydes de ces métaux, qui sont de couleur foncée.
E) Les métaux sont des éléments de couleurs variées et ternes, du fait de l'action de l'oxydation.
Résolution
Alternative E. Les métaux sont naturellement brillants et de couleur métallique, ils peuvent subir une oxydation, ce qui provoque des changements dans les caractéristiques pertinentes pour le aspect de la pièce, mais ce n'est pas un phénomène qui se produit dans tous les métaux, et, dans certains cas, l'oxydation dépend de plusieurs facteurs externe.
par Laysa Bernardes
Professeur de chimie


