Le texte "Molécule avec un carbone asymétrique et des isomères optiques” a montré que lorsqu'une molécule n'a qu'un seul carbone asymétrique ou chiral (avec tous les ligands différents l'un de l'autre), il possède deux isomères optiquement actifs et un isomère optiquement inactif (mélange racémique).
Considérons maintenant le cas où il existe au moins deux carbones asymétriques différents, c'est-à-dire qu'ils sont considérés comme différents les uns des autres car au moins un de leurs ligands n'est pas le même. Par exemple, considérons la formule de l'aspartame, qui est 180 fois plus sucré que le saccharose (sucre) et est donc utilisé dans les édulcorants artificiels :
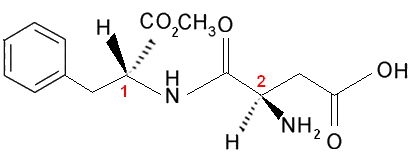
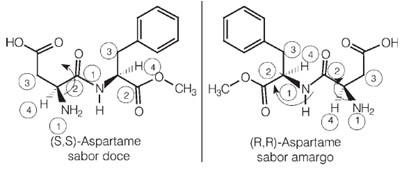
Notez que cette molécule a deux carbones chiraux, qui sont identifiés dans l'image par les numéros 1 et 2. Ces carbones ont leurs quatre groupes de liaison différents les uns des autres, ils sont donc considérés comme asymétriques. Lorsque l'on compare les ligands carbonés 1 avec ceux en carbone 2, on voit que le seul ligand répétitif est le H (hydrogène), étant donc des carbones asymétriques différents.
Cette molécule et toutes celles qui ont deux carbones asymétriques auront toujours: 4 isomères optiquement actifs et 2 isomères optiquement inactifs (deux mélanges racémiques).
Nous le savons car les probabilités possibles sont :

Toutes les autres paires d'isomères seront des diastéréoisomères (qui ne sont pas des images miroir les unes des autres), comme un mélange de carbone 1 droitier et de carbone 2 droitier.
Cependant, ce serait très difficile si nous devions continuer à regarder toutes les possibilités pour chaque molécule, car beaucoup ont 3, 4, 5 carbones asymétriques ou plus.
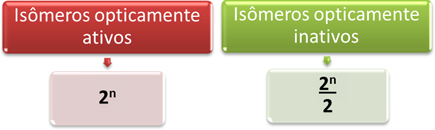
Ainsi, le moyen le plus simple de déterminer la quantité d'isomères optiquement actifs et inactifs d'une molécule qui a plusieurs différents carbones asymétriques est à travers les expressions mathématiques présentées ci-dessous qui ont été proposées par Van't Hoff et Le Bel :
Ne vous arrêtez pas maintenant... Y'a plus après la pub ;)
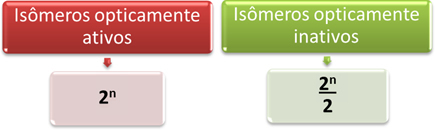
Où "n" est la quantité de carbones asymétriques différents dans la molécule. Par exemple, dans le cas de l'aspartame, ce sont deux carbones asymétriques, donc on a :
- Isomères optiquement actifs: 2non = 22 = 4;
- Isomères optiquement inactifs: 2non = 22 = 2.
2 2
Il a donné exactement le montant que nous avons mentionné précédemment.
Fait intéressant, l'un des énantiomères de l'aspartame a ce goût sucré qui est utilisé dans les édulcorants artificiels, mais l'un de ses isomères optiques a un goût amer.
Maintenant, regardons un autre exemple, la molécule de fructose :
OH OH OH OH OH
│ ║ │ │ │ │
H C C ─ Ç ─ Ç ─ Ç C ─ H
│ │ │ │ │
H OH H H H
Le fructose a trois atomes de carbone asymétriques, par conséquent, nous avons 8 isomères optiquement actifs et 4 isomères optiquement inactifs, qui sont 4 mélanges racémiques.
- Isomères optiquement actifs: 2non = 23 = 8;
- Isomères optiquement inactifs: 2non = 23 = 4.
2 2
Par Jennifer Fogaça
Diplômé en Chimie
Souhaitez-vous référencer ce texte dans un travail scolaire ou académique? Voir:
FOGAÇA, Jennifer Rocha Vargas. « Isomères dans des molécules avec différents carbones asymétriques »; École du Brésil. Disponible en: https://brasilescola.uol.com.br/quimica/isomeros-moleculas-com-carbonos-assimetricos-diferentes.htm. Consulté le 28 juin 2021.