Lorsque nous soumettons différents éléments à l'action d'une flamme, nous remarquons que chacun émet une couleur différente. Par exemple, si nous brûlons un sel de strontium, un sel de sodium et un sel de cuivre, nous verrons respectivement les couleurs rouge, jaune intense et vert, comme le montre la figure suivante :

Si la lumière de ces flammes tombe sur un prisme, un spectre discontinu, c'est-à-dire que seules quelques lignes lumineuses colorées seront observées entrecoupées de régions sans lumière. Pour chaque élément, nous aurons un spectre différent.

Ces types de spectres sont appelés Spectre d'émission, car ils ont été émis par un certain élément et servent à l'identifier.
Il est possible d'obtenir de tels spectres au moyen d'un faisceau lumineux produit dans un tube à décharge électrique à haute températures et basses pressions, contenant des gaz provenant de certains éléments tels que l'hydrogène, ou sous forme de gaz rares mugissement:

En faisant passer ce rayonnement électromagnétique (lumière) produit à travers un prisme, on obtient les spectres d'émission de chacun de ces éléments.
Auparavant, on pensait que le spectre solaire obtenu était totalement continu, mais le scientifique anglais William Hyde Wollaston a découvert qu'en en travaillant avec un faisceau lumineux très étroit, avec une fente d'environ 0,01 mm, on pouvait voir que le spectre solaire contenait sept raies noires à propos de ça. Plus tard, le jeune Joseph Fraunhofer (1787-1826), en utilisant des prismes et des réseaux de diffraction, a constaté que le spectre solaire contient en fait des milliers de raies noires superposées.
Quelque temps plus tard, le physique Gustav-Robert Kirchhoff il a remarqué que les taches jaunes, obtenues par le spectre du sodium, étaient exactement au même endroit que deux raies noires dans le spectre du Soleil. lui et le chimiste Robert Wilhelm Bunsen effectué plusieurs expériences et remarqué que si une lumière blanche du bec Bunsen, comme la lumière du soleil, passait par la lumière jaune émise par le sodium et le prisme était traversé pour générer le spectre; le résultat serait un spectre solaire continu, aux couleurs de l'arc-en-ciel, mais avec les lignes noires (appelées lignes D par Fraunhofer) dans la même position que les lignes jaunes dans le spectre du sodium.
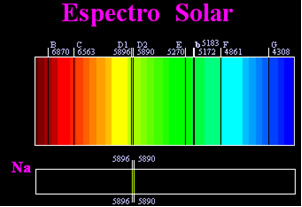
Le Soleil émet de la lumière de toutes les couleurs, du rouge au violet, cependant, en traversant l'atmosphère terrestre, les gaz présents absorbent la lumière du Soleil exactement dans les couleurs qu'ils émettent.
Ces types de spectres sont appelés spectres d'absorption.
Sur la base de ces observations, Kirchoff créé trois lois pour la Spectroscopie, qui sont :
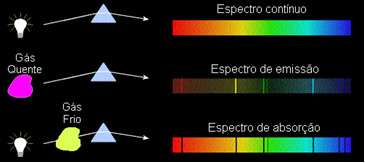
1) Un corps opaque chaud, dans l'un des trois états physiques, émet un spectre continu.
2) Un gaz transparent – comme ceux des gaz rares que nous avons vus ci-dessus – produit un Spectre d'émission, avec l'apparition de lignes brillant. Le nombre et la position de ces lignes seront déterminés par les éléments chimiques présents dans le gaz.
3) Si un spectre continu passe à travers un gaz à la température la plus basse, le gaz froid provoque la présence de lignes sombres, c'est un spectre d'absorption. C'est ce qui est arrivé au spectre de la lumière solaire traversant le sodium gazeux. Dans ce cas, le nombre et la position des raies dans le spectre d'absorption dépendent également des éléments chimiques présents dans le gaz.
Par Jennifer Fogaça
Diplômé en Chimie
La source: École du Brésil - https://brasilescola.uol.com.br/quimica/espectros-emissao-absorcao-leis-kirchhoff.htm

