Alkyynien hydraatio on vesimolekyylien additioreaktio happamassa väliaineessa katalyytin HgSO läsnä ollessa.4.
Nämä reaktiot ovat tärkeitä, koska niiden kautta on mahdollista saada aldehydejä ja ketoneja.
Aldehydiyhdisteet ovat orgaanisia yhdisteitä, joissa on vetyyn sitoutunut karbonyyliryhmä. Ketoneilla on toisaalta karbonyyliryhmä kahden hiilen välillä, kuten alla olevat funktionaaliset ryhmät osoittavat:
Aldehydit: Ketonit:
OO
║║
H - Ç ─ C ─ Ç ─C
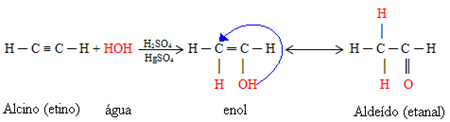
Jos hydraatioreaktion läpikäyvä alkyni on etaania, aldehydietanaali muodostuu. Aluksi muodostuu välituoteyhdiste, jolla on enolin yleisnimi.
Tämä enoli on erittäin epävakaa yhdiste, joka käy läpi molekyylimuutoksia korkean elektronegatiivisuuden takia. happi aiheuttaa elektronien vetovoiman hiilen kaksoissidoksesta, joka on heikko ja helppo sidos. liikkua. Tällä tavoin enoli ja aldehydi esiintyvät rinnakkain dynaamisessa tasapainossa. Tämä ilmiö on aldoenolisen tautomerian tapaus:
Älä lopeta nyt... Mainonnan jälkeen on enemmän;)
Kuitenkin, jos käytetään muuta alkiinia, jossa on vähintään kolme hiiltä, muodostuvat vastaavat ketonit. Tämä johtuu siitä, että tämä reaktio seuraa
Markovnikovin sääntö, jonka mukaan vedessä oleva vety lisää kolmoissidoshiiltä, jolla on eniten siihen sitoutuneita vetyjä, kun taas vedessä oleva OH sitoutuu kolmoissidokseen miinus hiili hydrattu.
Propanoni on asetonia, jota käytetään kynsilakan poistamiseen.
Kirjailija: Jennifer Fogaça
Valmistunut kemian alalta
Haluatko viitata tähän tekstiin koulussa tai akateemisessa työssä? Katso:
FOGAÇA, Jennifer Rocha Vargas. "Alkyynien nesteytys"; Brasilian koulu. Saatavilla: https://brasilescola.uol.com.br/quimica/hidratacao-alcinos.htm. Pääsy 28. kesäkuuta 2021.