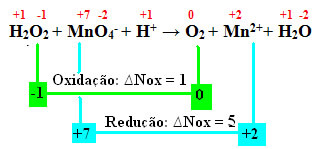
THE auto-oksi-pelkistys tai suhteeton reaktio on eräänlainen redoksireaktio, jossa sama kemiallinen alkuaine käy läpi hapettuminen ja vähentäminen. Tarkastellaan kahta esimerkkiä tämän tyyppisistä reaktioista ja siitä, kuinka tasapainottaa ne käyttämällä redox-menetelmää:
1. esimerkki:
AT2- + H+ → EI3- + NO + H2O
- Laskemalla kaikkien reaktiossa mukana olevien atomien ja ionien hapetusnumerot (NOX) on mahdollista tarkistaa, kuka hapettui ja kuka reagoi:
+3 -2 +1 +5 -2 +2 -2 +1 -2
AT2- + H+ → EI3- + NO + H2O
- Huomaa, että typpi oli laji, joka sekä reagoi että hapetti:
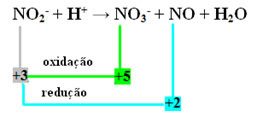
- Tämän reaktion redoksitasapainottamisen suorittamiseksi meidän on suhteutettava NOX tuotteisiin, ei reagensseihin:
AT3- = ∆Nox = 5 - 3 = 2
NO = ∆Nox = 3 - 2 = 1
- Kääntämällä ∆NOX kertoimilla, meillä on:
AT3- = ONOX = 2 → 2 on NO: n kerroin
EI = ∆NOKSI = 1→ 1 on NO: n kerroin3-
AT2- + H+ → 1 AT3- + 2 NO + H2O
- Tämän avulla tiedämme jo, että tuotteessa on 3 N, joten NO-kerroin2- on 3:
3 EI2- + H+ → 1 EI3- + 2 NO + H2O
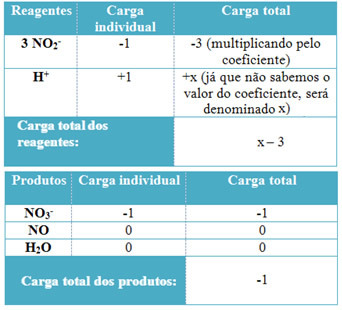
- H-kertoimien määrittämiseksi + ja H: ltä2O, muista, että vastaanotettujen elektronien lukumäärä on sama kuin luovutettujen elektronien määrä; siten reagenssipanos on yhtä suuri kuin tuotteen panos. Tällä tavalla voimme tehdä seuraavan kaavan:
Älä lopeta nyt... Mainonnan jälkeen on enemmän;)
Näiden tietojen perusteella meillä on, että reagenssien kokonaismäärä on yhtä suuri kuin x - 3 ja tuote on yhtä suuri kuin -1. Kuten todettiin, näiden kahden maksujen on oltava samat. Koska meillä on jo tuotteiden kokonaiskuormitus, voimme suorittaa yksinkertaisen laskutoimituksen, jotta tiedämme, mikä on x: n arvo:
x -3 = -1
x = -1 +3
x = 2
Siten H-kerroin+ on 2 ja näin ollen H: n2Tulee olemaan 1:
3 EI2- + 2 H+ → 1 EI3- + 2 NO + 1 H2O
2. esimerkki:
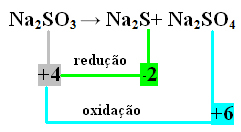
Tässä tapauksessa S: lle tehtiin pelkistys ja hapetus samanaikaisesti. Siten, kuten aiemmin on tehty, voimme liittää NOX: n tuotteisiin ja kääntää niiden arvot osoittamalla heille kertoimet:
Klo2 S = ∆Nox = 4 - (-2) = 6 → 6 on Na-kerroin2 VAIN4
Klo2 VAIN4= ∆Nox = 6-4 = 2 → 2 on Na-kerroin2 s
Klo2 VAIN3→ 2 Klo2 Y + 6 Klo2 VAIN4
Koska 2. raajassa on 8 rikkiä, Na-kerroin2 VAIN3 tulee olemaan 8:
8 tuumaa2 VAIN3→ 2 tuumaa2 S + 6 tuumaa2 VAIN4
Kirjailija: Jennifer Fogaça
Valmistunut kemian alalta
Haluatko viitata tähän tekstiin koulussa tai akateemisessa työssä? Katso:
FOGAÇA, Jennifer Rocha Vargas. "Itsehapetusreaktiot"; Brasilian koulu. Saatavilla: https://brasilescola.uol.com.br/quimica/reacoes-auto-oxirreducao.htm. Pääsy 28. kesäkuuta 2021.