Ymmärtääksemme, miksi kun poltamme puuta, se ei sula, muistetaan ensin, mikä on sula aine eli se on nestemäisessä tilassa.
Kiinteiden, nestemäisten ja kaasumaisten tilojen ero on vain hiukkasten aggregaatiotilassa. Kolmessa tilassa aine koostuu samoista hiukkasista, mutta niiden välillä on enemmän tai vähemmän tilaa.
Kiinteässä tilassa hiukkaset ovat lähempänä toisiaan ilman suurta liikkumisvapautta. Nestemäisessä tilassa hiukkasilla on enemmän vapautta ja ne voivat liikkua.
On käynyt ilmi, että suuri osa puusta (50%) on valmistettu selluloosasta, joka on itse asiassa polymeeri. Polymeeri muodostuu yhdistämällä useita molekyylejä, joita kutsutaan monomeereiksi. Selluloosan tapauksessa se muodostuu satojen p-glukoosimolekyylien liittymisestä, kuten alla on esitetty. Selluloosalla on sitten kaava (C6H10O5)ei ja saavuttaa molekyylimassat luokkaa 400 000 u.
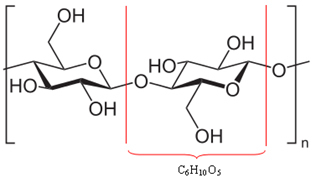
Koska ne ovat valtavia molekyylejä, nämä puun muodostavat polymeerit eivät voi liikkua helposti. Huomaa myös, että selluloosaa muodostavilla β-glukoosimolekyyleillä on hydroksyyliryhmiä (─ OH). Nämä ryhmät sitovat vetyä toisiinsa, mikä on voimakkain molekyylien välinen voima, joka pitää polymeerin tiukasti yhdessä.

Vetysidokset selluloosapolymeerin muodostavien molekyylien välillä *
Täten, näiden sidosten rikkomiseksi meidän olisi lisättävä järjestelmään niin paljon energiaa, että puu hajoaa jo ennen kuin se sulaa eikä ole enää puuta.
Siten poltettaessa puu puuttuu kemiallisessa reaktiossa, mikä on muutakin kuin yksinkertainen fyysisen tilan muutos. Sen molekyylit hajoavat ja yhdistyvät uudelleen ilmassa olevan hapen kanssa ja muodostavat sitten uusia aineita, kuten hiilikaasua ja vettä.

* Lähde ja kuvan kirjoittaja: laghi.l.
Kirjailija: Jennifer Fogaça
Valmistunut kemian alalta
Lähde: Brasilian koulu - https://brasilescola.uol.com.br/quimica/por-que-madeira-nao-derrete.htm
